ʱ��:2019-07-04 01:54:53
1��ѡ���� ��298K��1.01��105Pa�£���22g CO2ͨ��1mol��L-1 NaOH��Һ750mL�г�ַ�Ӧ����÷�Ӧ�ų�x kJ����������֪�������£�1mol CO2ͨ��2mol��L-1 NaOH��Һ1L�г�ַ�Ӧ�ų�y kJ����������CO2��NaOH��Һ��Ӧ����NaHCO3���Ȼ�ѧ����ʽ��ȷ����
[? ]
A��CO2��g��+NaOH��aq��=NaHCO3��aq�� ��H=����2y��x��kJ��mol-1
B��CO2��g��+NaOH��aq��=NaHCO3��aq�� ��H=����2x��y��kJ��mol-1
C��CO2��g��+NaOH��aq��=NaHCO3��aq�� ��H=����4x��y��kJ��mol-1
D��2CO2��g��+2NaOH��aq��=2NaHCO3��aq�� ��H=����8x��2y��kJ��mol-1
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� ��֪:
��NH3(g)+HCl(g)==NH4Cl(s) ��H1=-176 kJ��mol-1
��NH3 (g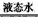 (aq) ��H2=-35.1 kJ��mol-1
(aq) ��H2=-35.1 kJ��mol-1
��HCl(g) HCl(aq) ��H3=-72. 3 kJ��mol-1
HCl(aq) ��H3=-72. 3 kJ��mol-1
��NH3 (aq) +HCl(aq)==NH4Cl(aq) ��H4=-52. 3 kJ��mol-1
��NH4Cl(s) NH4Cl(aq) ��H5
NH4Cl(aq) ��H5
��ڢݸ��Ȼ�ѧ����ʽ�С�H5Ϊ
[? ]
A. +16.3 kJ��mol-1
B. -16.3 kJ��mol-1
C. +335.7 kJ��mol-1
D. -335.7 kJ��mol-1
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3������� ��������������Ӧ����1molˮ��������241.8KJ����֪������H-H����Ϊ436kJ/mol������������O=O����Ϊ498kJ/mol����ˮ������O-H���ļ���Ϊ______kJ/mol����1gˮ����ת����Һ̬ˮʱ����2.5kJ����ӦH2��g��+1/2O2��g���TH2O��l���ġ�H=______kJ/mol��
�ο��𰸣�������������Ӧ����1molˮ��������241.8kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ��H2��g��+12O2��g��=H2O��g����H=-241.8kJ/mol����Ӧ���ܼ���-�������ܼ���=��Ӧ�ȣ���
436kJ/mol+12��498kJ/mol-2E��O-H��=-241.8kJ/mol����E��O-H��=463.4kJ/mol��
1gˮ����ת����Һ̬ˮʱ����2.5kJ��1molˮ����ת��ΪҺ̬ˮ�ų�������Ϊ1mol��18g/mol1g��2.5kJ=45kJ��������1molҺ̬ˮ�ų�������Ϊ241.8kJ+45kJ=286.8kJ����H2��g��+1/2O2��g���TH2O��l���ķ�Ӧ�ȡ�H=-268.8kJ/mol��
�ʴ�Ϊ��463.4kJ/mol��-268.8kJ/mol��
���������
�����Ѷȣ�һ��
4��ѡ���� ����˵�����ʾ��������ȷ����
[? ]
A�����������������������ֱ���ȫȼ�գ����߷ų���������
B����֪C(s)+1/2O2(g)=CO(g)�ķ�Ӧ��Ϊ110��5kJ/mol��˵��̼��ȼ����Ϊ110��5kJ
C��ij�¶��£����һ�����ܱ������н������¿��淴Ӧ��X���磩��Y���磩 Z���磩��W����
Z���磩��W����
���ȣ�0����ƽ������أ���������Ӧ�Ħ�������
D��ϡ��Һ�У�H+��aq��+OH-��aq)=H2O(l) ��H= -53��7kJ��mol-1��������0��5molH2SO4��Ũ��Һ�뺬
1molNaOH����Һ��ϣ��ų�����������53��7KJ
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ��100g̿����ȫȼ������������CO��CO2�������Ϊ1��2����֪��C��s��+
| 1 2 |
| 1 2 |
�ο��𰸣�C
���������
�����Ѷȣ�һ��