���ۣ�д�ṹ��ʽ����
�˴Ź���������1����
______?
�˴Ź���������3����
______?
�ο��𰸣���1����3.6gˮ�����ʵ���Ϊ3.6g18g/mol=0.2mol����n��H��=0.2mol��2=0.4mol��m��H��=0.4mol��1g/mol=0.4g��3.36L����״���£�CO2�����ʵ���Ϊ3.36L22.4L/mol=0.15mol����n��C��=0.15mol��m��C��=0.15mol��12g/mol=1.8g������0.4g+1.8g=2.2g��3.6g����m��O��=3.6g-0.4g-1.8g=2.4g��n��O��=2.4g16g/mol=0.15mol����n��C����n��H����n��O��=0.15mol��0.4mol��0.15mol=3��8��3����ʵ��ʽΪC3H8O��
�ʴ�Ϊ��C3H8O��
��Hԭ���Ѿ����ͣ����ʽ��Ϊ����ʽ�����л������ʽΪC3H8O��
�ʴ�Ϊ��Hԭ���Ѿ����ͣ����ʽ��Ϊ����ʽ��
�������ʵ���һ��������£����л����ij��̬���Ļ��������Ժα�����ϣ���ȫȼ�������ĵ�������������ҲΪ��ֵ��˵��1molC3H8O�������ĵ����������ʵ�����ȣ���C3H8O��дΪC3H6?H2O���ʸ���ΪC3H6���ϣ�
�ʴ�Ϊ��C3H6��
��2����Ũ��������5.4g��ˮ��������ˮ�����ʵ���Ϊ5.4g18g/mol=0.3mol������Hԭ���غ���n��H��=2n��H2O��=0.6mol����ʯ������4.4g�����ɵĶ�����̼��������������̼�����ʵ���Ϊ4.4g44g/mol=0.1mol�����������ʵ���Ϊ5.6L22.4L/mol=0.25mol������������Ϊ0.25mol��32g/mol=8g�����������غ��֪CO������Ϊ4.6g+8g-5.4g-4.4g=2.8g��CO�����ʵ���Ϊ2.8g28g/mol=0.1mol������Cԭ���غ���n��C��=n��CO2��+n��CO��=0.1mol+0.1mol=0.2mol��
�ʴ�Ϊ��0.6?mol��0.2?mol��
��m��H��=0.6mol��1g/mol=0.6g��m��C��=0.2mol��12g/mol=2.4g����m��O��=4.6g-0.6g-2.4g=1.6g��n��O��=1.6g16g/mol=0.1mol����n��C����n��H����n��O��=0.2mol��0.6mol��0.1mol=2��6��1����ʵ��ʽΪC2H6O��Hԭ���Ѿ����ͣ����ʽ��Ϊ����ʽ��
�ʴ�Ϊ��C2H6O��
��3�����˴Ź���������1���壬������Hԭ�ӵ�Ч�����л���Ľṹ��ʽΪCH3OCH3��
���˴Ź���������3���壬˵����������3�ֲ���ЧHԭ�ӣ����л���Ľṹ��ʽΪCH3CH2OH��
�ʴ�Ϊ��CH3OCH3��CH3CH2OH��
���������
�����Ѷȣ�һ��
2���ƶ��� ϩ��A��һ�������¿�����ͼ���з�Ӧ

��֪����1��F1��F2��Ϊͬ���칹�壬?G1��G2��Ϊͬ���칹�塣
��2��D�� ? ?
����գ�
��1�����Ľṹ��ʽ�ǣ�______________��
��2����ͼ������ȡ����Ӧ����(�����ִ���)��_____________����ͼ�Т٢ۢ�����____________��Ӧ��
��3��G1�Ľṹ��ʽ�ǣ�___________��
��4��д����Ӧ�ڵĻ�ѧ����ʽ__________ д����Ӧ�ݵĻ�ѧ����ʽ______________����������?������������
�ο��𰸣���1��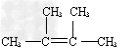 ? ?
��2����?���ӳ�
��3��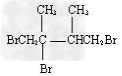 ? ?
��4�����ԡ�
���������
�����Ѷȣ�һ��
3������� (15��)�߾���E�dz�����һ�������ϰ�װ������Ҫ�ɷ֣����ĺϳ�·�����£�

��ش��������⣺
��1����֪����A������������������ܶ�Ϊ39����A�����ʽΪ? ��?��
��2����A����B�ķ�Ӧ������? ��?��д����C����D�ķ���ʽ? ��?��
��3����֪������G(C8H6O4)��B��һ��ͬ���칹�������Ը��������Һ��Ӧ��IJ��G�ĺ˴Ź�������������壬�ҷ������Ϊl��2��д��G�Ľṹ��ʽ? ��?��
��4����F��ͬ���칹���У����������Ĺ���? ��?�֡�
��5��һ�������ϰ�װ���������������������ͬʱҲ�����ˡ���ɫ��Ⱦ��������ҹ���ѧԺ����ѿΪԭ�ϣ����Ƴ���һ�����߷��ӿɽ������ϨD�D�۶�����(��ṹ�� )�����ɴ���߾���E���Լ��١���ɫ��Ⱦ�����۶��������û������������ۺ϶��ɣ��乤ҵ���������ͽ���ԭ�����£� )�����ɴ���߾���E���Լ��١���ɫ��Ⱦ�����۶��������û������������ۺ϶��ɣ��乤ҵ���������ͽ���ԭ�����£�

��д�����������Ľṹ��ʽ��? ��??��
��д��ͼ�Тٵ���Ӧ��ѧ����ʽ??��??��
��I��һ�������¿��Ժϳ�һ����Ҫ����ԭ��J��

д����I�ϳ�J��·������ͼ�����Լ���ѡ����
�ϳ�·������ͼ��дʾ�����£�
�ο��𰸣���15�֣���1��CH (1��) ��2���ӳɷ�Ӧ(1��)��
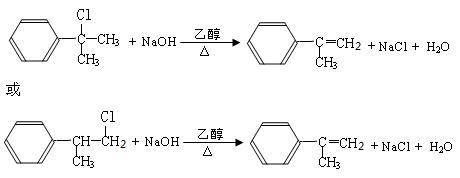 ��2�֣� ��2�֣�
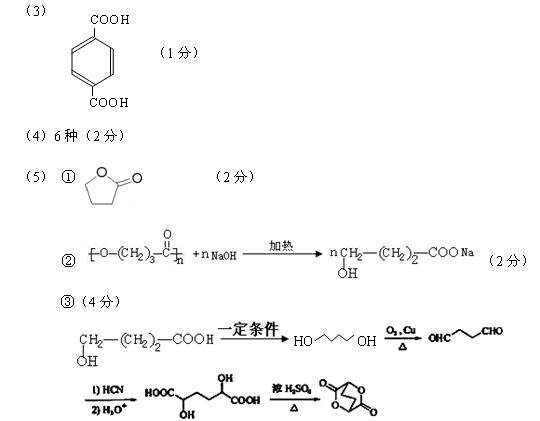
���������𰸾��ɸ��֡�©д��Ӧ����ÿ1���0.5�֣����1��۷֣�3���1�֣��������ּ��롣�л���ṹ��ʽÿ��1����1�֣����۷ֲ�����4�֣�
�����������
�����Ѷȣ���
4������� ��14�֣�ij�л����A��Ϊͬ���칹�壬���ⶨ���ǵ���Է�������С��100����1mol����O2�г��ȼ�յõ������ʵ�����CO2��H2O (g) ��ͬʱ����112LO2����״�����������������½�1 mol����ȫˮ���������1 mol �Һ�1mol����������һ�������£������Ա�����������Ϊ�ҡ�

��������ײⶨ���ڼ�A�Ľṹ�ж�����C��O˫����C��O������B��HIO4���ڲ�����ʱֻ����һ�� ����C������Ϊ����ط�Ӧ����Ϣ��ת����ϵ�� ����C������Ϊ����ط�Ӧ����Ϣ��ת����ϵ��

�� ��ȷ����д���ķ���ʽ? ��?�������ͬ�����ʵ�ͬ���칹�干��? ��?�֣������ף���
�� E �� F �ķ�Ӧ����Ϊ? ��?��Ӧ��
�� A�Ľṹ��ʽΪ? ��?��G �Ľṹ��ʽΪ? ��?��
�� B ��D�ķ�Ӧ��ѧ����ʽΪ? ��?��
�� д��C���������½��з�Ӧ�Ļ�ѧ����ʽ? ��?��
�ο��𰸣���14�֣�
�� C4H8O2��2�֣�? 4 ��2�֣�?����ȥ��Ӧ��2�֣�
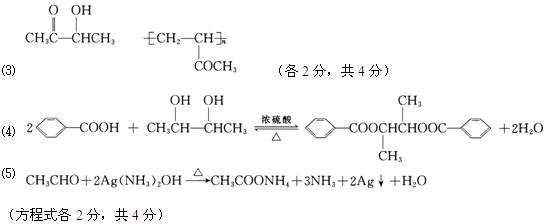
�����������
�����Ѷȣ�һ��
5���ƶ��� �л���E��C6H8O4���㷺����Ϳ����ҵ�У���ϳ�·�����£�����ֱ����A����Է���������56��B����Է���������A��69����

��1����A�Ľṹ��ʽΪ________________��
��2���۵ķ�Ӧ������______________��Ӧ��
��3������˵����ȷ����___________������ţ���
a.��Ӧ������ȡ����Ӧ? b.B����ȼ��黥Ϊͬϵ��
c.C��������������ͬ���칹��? d.D�ܷ������۷�Ӧ
��4��Cת��ΪD��������4����Ӧ��ɣ�  D�� D��
�����������Լ�����Ӧ������___________���ܵĻ�ѧ����ʽ��_________________��
�ο��𰸣���8�֣���1��CH3CH��CHCH3��1�֣� ��2��ȡ��������������1�֣� ��3��ad��2�֣�ѡ��1����1�֣��д��÷֣� ��4��NaOH����Һ�����ȣ�ȫ��2�֣��д��÷֣�
HOCH2��CH��CH��CH2OH��HCl HOCH2CH2CHClCH2OH��2�֣� HOCH2CH2CHClCH2OH��2�֣�
������������ݷ�Ӧ������֪����Ӧ����±������ˮ�ⷴӦ����C�Ǵ��ࡣ��ת����ϵ��C�ķ���ʽC4H8O2��֪��A�����к���4��̼ԭ�ӡ�����Ϊֱ����A����Է���������56������A�к��е���ԭ����ĿΪ��56��4��12����1��8�����A�Ļ�ѧʽ��C4H8����ת����ϵ��֪��BΪ�ȴ�����B����Է���������A��69�����BΪ��Ԫ�ȴ�������CΪ��Ԫ������C��D��C4H4O4���ķ���ʽ��֪��C����������Ӧ����D��D�ܺͼ״���Ũ����������·���������Ӧ������D�Ƕ�Ԫ���ᡣ����D�Ļ�ѧʽ��֪��D�IJ����Ͷ�Ϊ��4��2��2��4����2��3������D�к���̼̼˫�������D�Ľṹ��ʽΪHOOC-CH��CH-COOH�����ƿ�֪��CΪHOCH2��CH��CH��CH2OH��BΪClCH2��CH��CH��CH2Cl��AΪCH3CH��CHCH3��D��CH3OH��Ũ���ᡢ���������·���������Ӧ����E��C6H8O4������E�Ľṹ��ʽΪCH3OOC��CH��CH��COOCH3��
��1��������������֪����A�Ľṹ��ʽΪCH3CH��CHCH3��
��2����Ӧ����HOOC��CH��CH��COOH��CH3OH��Ũ���ᡢ���������·���������Ӧ����E��C6H8O4��������ȡ����Ӧ��
��3��a����Ӧ����CH3CH��CHCH3��������Ӧ����ClCH2-CH=CH-CH2Cl������ȡ����Ӧ����a��ȷ��b��B�к���̼̼˫��������ȼ��鲻��ͬϵ���b����c��C����������ͬ���칹�壬��CH3CH2CH2COOH�ȣ���c����d��D�����к���2����COOH���ܷ������۷�Ӧ����d��ȷ����ѡad��
��4��Cת��ΪD��������4����Ӧ��ɣ�  D����Ӧ����HCl�����ӳɷ�Ӧ������̼̼˫�������Ը��������������Ӧ����ʽΪ��HOCH2��CH��CH��CH2OH��HCl D����Ӧ����HCl�����ӳɷ�Ӧ������̼̼˫�������Ը��������������Ӧ����ʽΪ��HOCH2��CH��CH��CH2OH��HCl
 HOCH2CH2CHClCH2OH����Ӧ�����������ƴ���Һ�����������·�����ȥ��Ӧ����ԭ̼̼˫���� HOCH2CH2CHClCH2OH����Ӧ�����������ƴ���Һ�����������·�����ȥ��Ӧ����ԭ̼̼˫����
�����Ѷȣ�����
|