时间:2019-07-04 01:31:28
1、选择题 下列物质中,既含有离子键又含有共价键的是
A.CH4
B.NaOH
C.SO2
D.H2O
参考答案:B
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。据此判断A~D中含有的化学键分别是极性键、离子键和极性键、极性键、极性键,所以答案选B。
本题难度:一般
2、选择题 2g碳与水蒸气反应生成CO和H2,需吸收21.88kJ热量,此反应的热化学方程式为 ( )
A.C + H2O ==CO + H2ΔH==+131.3kJ·mol—1
B.C(s)+ H2O(g) ==CO(g) + H2(g)ΔH==+10.94kJ·mol—1
C.C(s)+ H2O(g) ==CO(g) + H2(g)ΔH==-131.3kJ·mol—1
D.C(s)+ H2O(g) ==CO(g) + H2(g)ΔH==+131.3kJ·mol—1
参考答案:D
本题解析:略
本题难度:一般
3、填空题 (9分)发射卫星时可用肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知:N2(g) +2 O2(g) = 2NO2(g);△H=+67.7kJ·mol-1
N2H4(g) + O2(g) = N2(g) + 2H2O(g);△H=-534kJ·mol-1
1/2H2(g) + 1/2F2(g) = HF(g);△H=-269kJ·mol-1
H2(g) + 1/2O2(g) = H2O(g);△H=-242kJ·mol-1
(1)肼和二氧化氮反应的热化学方程式为 ;此反应用于火箭推进,除释放大量能量和快速产生气体外,还有一个很大的优点是:__________ 。
(2)有人认为若用氟气代替二氧化氮作氧化剂,则反应释放的能量更大。肼和氟气反应的热化学方程式为 ___。
参考答案:(1) N2H4(g) + NO2(g) = 3/2 N2(g) + 2H2O(g) △H=-567.9kJ·mol-1
产物为N2和H2O,对环境无污染。
(2) N2H4(g) +2 F2(g) = N2(g) + 4 HF(g);△H=-1126kJ·mol-1
本题解析:(1)考查盖斯定律的应用。根据反应①N2(g) +2 O2(g) = 2NO2(g)和反应②N2H4(g) + O2(g) = N2(g) + 2H2O(g)可知,②-1/2①即得到 N2H4(g) + NO2(g) = 3/2 N2(g) + 2H2O(g),所以反应热是
本题难度:一般
4、选择题 金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。?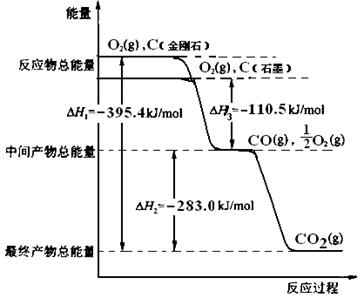
(1)等量金刚石和石墨完全燃烧__________(填“金刚石”或“石墨”)放出热量更多,写出表示石墨燃烧热的热化学方程式___________________________________。
(2)在通常状况下,金刚石和石墨__________(填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石的热化学方程式___________________________。
(3)12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量?。
参考答案:(1)金刚石(1分) C(石墨s)+O2(g)=CO2(g);△H=-393.5kJ/mol(2分)
(2)石墨(1分)C(石墨s)= C(金刚石s);△H="+1.9" kJ/mol(2分)
(3)252.0kJ(3分)
本题解析:(1)从图像上很显然可以看出金刚石能量比石墨高,所以等量金刚石和石墨完全燃烧金刚石放出热量更多,根据燃烧热定义,石墨完全燃烧生成二氧化碳,根据图像反应放出的总热量为110.5+283.0=393.5kJ,所以,表示石墨燃烧热的热化学方程式为C(石墨s)+O2(g)=CO2(g);△H=-393.5kJ/mol(2)因为金刚石能量比石墨高,根据能量越低越稳定,所以在通常状况下石墨更稳定。石墨转化为金刚石要吸收热量,1mol石墨转化为金刚石吸收热量395.4-393.5=1.9kJ,热化学方程式为C(石墨s)= C(金刚石s);△H="+1.9" kJ/mol
(3)12g石墨在一定量空气中燃烧,生成气体36g,根据碳原子守恒,气体总物质的量为1mol,所以生成气体平均摩尔质量为36g/mol,利用十字交叉法求算混合气体中CO和CO2的物质的量的比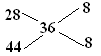 所以混合气体中CO和CO2各0.5mol,该过程放出热量为110.5+283.0/2=252.0kJ。
所以混合气体中CO和CO2各0.5mol,该过程放出热量为110.5+283.0/2=252.0kJ。
本题难度:简单
5、选择题 关于化学反应中的说法错误的是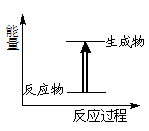
A.化学键断裂吸收能量,化学键生成放出能量
B.化学反应中有物质变化也有能量变化
C.上图所示的反应为放热反应
D.需要加热的化学反应不一定是吸热反应
参考答案:C
本题解析:A.化学键断裂吸收能量,化学键生成放出能量,正确;B.化学反应的过程就是原子重新组合的过程,在这个过程中断裂反应物中的化学键吸收能量,形成生成物中的化学键要释放能量,因此化学反应中有物质变化也有能量变化,正确;C.在右图所示由于反应物的能量低,生成物的能量该,所以反应发生时要吸收能量,因此该反应为吸热反应,错误;D.任何反应发生都需要一个活化的过程,所以需要加热的化学反应不一定是吸热反应,正确。
考点:考查化学反应过程中的物质变化与能量变化的关系的知识。
本题难度:一般