时间:2019-07-04 00:54:31
1、填空题 已知:反应AsO43- + 2I- + 2H+ AsO33- + I2 + H2O 是可逆反应,现设计如下装置,进行操作:
AsO33- + I2 + H2O 是可逆反应,现设计如下装置,进行操作:
①操作向烧杯中逐滴滴加浓硫酸,电流表指针偏转;
②操作再取相同的另一装置,向烧杯中逐滴滴加40%NaOH溶液,电流表指针向①中指针偏向相反的方向偏转;
回答下列问题
(1)从能量变化的角度分析,两次操作过程中指针发生偏转的原因是_______________
(2)用化学平衡移动原理解释,两次操作过程中指针偏转方向相反的原因是______________
(3)操作①过程中负极发生的电极反应式为__________________
操作②过程中负极发生的电极反应式为________________
2、简答题 现有如下两个反应:(A)NaOH+HCl=NaCl+H2O? (B)2FeCl3+Cu=2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池______
(2)如果不能,说明其原因______
(3)如果可以,请写出正负极材料名称和电极反应式.
______是正极,正极反应式:______
______是负极,负极反应式:______.
3、选择题 有关右图装置,描述正确的是(?)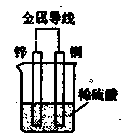
A.电流从锌电极经金属导线流向铜电极
B.锌为阴极,铜为阳极
C.负极的电极反应式为:Zn—2e→Zn2+
D.一段时间后,溶液中阳离子浓度增大、阴离子浓度不变
4、选择题 在理论上不能用于设计原电池的化学反应是
[? ]
A.HCl(aq)+ NaOH(aq)=== NaCl(aq)+ H2O(l) △H < 0
B.2CH3OH(l)+3O2(g)=== 2CO2(g)+ 4H2O(l) △H < 0
C.Zn(s)+CuSO4(aq)=== ZnSO4(aq)+Cu(s) △H < 0
D.2H2(g)+ O2(g)=== 2H2O(l) △H < 0
5、选择题 下列各组电极均用导线相连,分别插入对应溶质的溶液中,其中不能组成原电池的是
| ? | A | B | C | D |
| 电极与溶液 | Zn、C 硫酸 | Cu、Ag 硝酸银 | Mg、Al 盐酸 | Zn、Cu 蔗糖 |