ʱ��:2019-07-03 23:53:44
1��ѡ���� ���������У�������ϡ���ᷴӦ������������������Һ��Ӧ����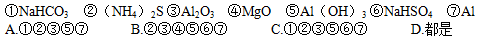
�ο��𰸣�A
���������������ϡ���ᷴӦ������������������Һ��Ӧ������һ��������������������������������Ρ���Ԫ�������ʽ�Σ���ΪA
�����Ѷȣ�һ��
2������� ��1���֣�
һλͬѧ�ڸ�ϰʱ��������һ��ϰ�⣺ij��ɫ��Һ�п��ܺ��С�H+��OH-��Na+��NO3-�����������ۺ�ֻ����H2���ʸ���ɫ��Һ���ܴ��������ļ������ӡ�
��1���������۲���H2��˵��������______��������ԡ���ԭ�ԡ�����
��2����ͬѧ��������H+�������ڣ���NO3-�Ͳ��ܴ������ڡ�
���ʵ��֤ʵ���£�
| װ �� | �� �� |
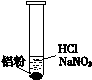 | ��. ʵ���ʼ��δ���������� ��. ��һ������������ݣ�Һ���Ϸ���dz��ɫ ��. �Թܱ��ȣ���Һ���� |
| ʵ?�� | ��?�� | ��?�� |
| ʵ��1 | ?��ʪ��KI��������ֽ���ڿ����� | δ���� |
| ʵ��2 | ��ʪ��KI��������ֽ����dz��ɫ���� | ��ֽ���� |
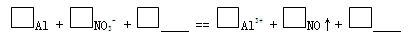
| װ �� | �� �� |
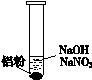 | ��. ʵ���ʼ��δ���������� ��. ��һ������������ݣ��д̼�����ζ |
�ο��𰸣���1���֣�
��1����ԭ��
��2���� 6H+ + Al2O3 ="=" 2Al3+ + 3H2O
�� a.NO2
b. �Ա�ʵ�飬�ų�����ʹʪ��ĵ���KI��ֽ�����Ŀ���
c. 1��1��4H+��1��1��2H2O
��3���� NH3
�� 8Al +3NO3- + 5OH-+ 2H2O ="=" 3NH3��+ 8AlO2-
��4��2Al +2NaOH + 2H2O ="=" 2NaAlO2 + 3H2��
�����������1���������۲���H2��˵�������л�ԭ�ԣ�
��2���� �����ܽ�Al2O3��Ĥ�������Ȼ�����ˮ�����ӷ���ʽΪ6H+ + Al2O3 ="=" 2Al3+ + 3H2O
��a.��dz��ɫ������NO2
b��ʵ��1��Ŀ������ʵ��2���Աȣ��ų�ʵ��2������ʹʪ��ĵ���KI��ֽ�����Ŀ��ܣ�
c��������ѧ֪ʶ��Al�����ᷴӦ����NO�����Է�Ӧ��Ŀհ�Ӧ��д��H+�������Բ�����Ӧ��ˮ���ڣ��ٸ��ݵ�ʧ�����غ㷨���۲취��ƽ����ʽ���ɡ���ƽ������ӷ���ʽΪ��Al+NO3-+4H+=Al3++NO��+2H2O
��3������ʪ���ɫʯ����ֽ���飬��ֽ��������ʹʪ���ɫʯ����ֽ������������NH3��
�� �÷�Ӧ�а���������˵��Al������������Һ����������Һ������������ԭ��Ӧ�����ӷ���ʽΪ��8Al +3NO3- + 5OH-+ 2H2O ="=" 3NH3��+ 8AlO2-��
��4��Al�뵥һ����������Һ��Ӧ�Ļ�ѧ����ʽ��2Al +2NaOH + 2H2O ="=" 2NaAlO2 + 3H2����3-�������Ե��жϣ������ļ��飬��ѧ����ʽ�����ӷ���ʽ����д
�����Ѷȣ�һ��
3��ѡ���� ���ֱ����������������ƺ�ϡ������Һ��Ӧ����������Ӧ�ų�����������ͬ״����������ʱ����Ӧ�����ĵ�NaOH��HCl���ʵ���֮��Ϊ��������
A��2��1
B��3��1
C��1��1
D��1��3
�ο��𰸣������ɵ����������ʵ���Ϊ3mol����
? 2Al+6HCl=2AlCl3+3H2����
?6mol? 3mol
2Al+2NaOH+2H2O=2NaAlO2+3H2��
? 2mol?3mol
������ȡ�������ƺ�������Һ��NaOH��HCl�����ʵ�����֮��Ϊ2mol��6mol=1��3��
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� ���������У�����������������NaOH��Һ��Ӧ����
A.��������
B .������
C.̼����
D.��������
�ο��𰸣�A
����������������������ʼ�ķ�Ӧ�����жϣ���ѧ�����ļ������ᷴӦ������Ӧ��������Ҫ�У�
���������ʣ�Al2O3��ZnO��Al��OH��3��Zn��OH��2�������ᡢ�����ʵȣ�
�ڶ�Ԫ�������ʽ�Σ�NaHCO3��KHS��KHSO3��NaH2PO4�ȣ�
���������μ�����ʽ�Σ���NH4��2S��NH4HS����NH4��2CO3��NH4HCO3��CH3COONH4�ȣ�
��ijЩ�������ԵĽ�����Zn��Al�ȣ�
��ijЩ�ǽ�����Si��S�ȣ�
������һЩ���ʣ��磺a��ijЩ�������ʼ����ᷴӦ������Ӧ��
b����������������SiO2��
c�����л�ԭ�Ե������H2S��HI�����������ᷴӦ����Ӧ��
d�������������ŨH2SO4��HNO3���뻹ԭ���ᷴӦ����Ӧ���Դ˽���⣮
���A������������������������������ᷴӦ�����Ȼ�����ˮ�����������Ʒ�Ӧ����ƫ��������ˮ����A���ϣ�
B�������������ᷴӦ���ɹ������Ȼ��ƣ��������������Ʒ�Ӧ����B�����ϣ�
C��̼���������ᷴӦ�����Ȼ��ơ�������̼��ˮ���������������Ʒ�Ӧ����C�����ϣ�
D�������������������Ʒ�Ӧ���ɹ�������ˮ�����������ᷴӦ����D�����ϣ�
��ѡA��
���������⿼�������ʵ����ʣ��ѶȲ���ּ�ڿ���ѧ����֪ʶ������ʶ����֪ʶ���ɣ���ȷ���ʵ������ǽⱾ��Ĺؼ���ע�����֪ʶ�Ļ��ۣ�
�����Ѷȣ���
5������� ��16�� ��þ���������������ɺϽ�þ���Ͻ��ǿ�ȸߣ���е���ܺá��С���������������������Ȼ���е�þԪ����Ҫ�����ں�ˮ�С���ˮ��þ���ܴ���ԼΪ1.8��1015?t���Ӻ�ˮ�У���Ҫ����Na+��Cl����Mg2+�����ӣ���ȡþ�Ĺ�������ͼ���£�
��þ���������������ɺϽ�þ���Ͻ��ǿ�ȸߣ���е���ܺá��С���������������������Ȼ���е�þԪ����Ҫ�����ں�ˮ�С���ˮ��þ���ܴ���ԼΪ1.8��1015?t���Ӻ�ˮ�У���Ҫ����Na+��Cl����Mg2+�����ӣ���ȡþ�Ĺ�������ͼ���£�
��1��A���ʵĻ�ѧʽΪ?������1������Ϊ?��
��2����д�������A�м���������������ӷ���ʽ?��
��3���÷�Ӧ�ĸ�������Ҫ��?�ȡ�
��4������ʼ�õ��Ĺ���A������Ϊ116g�����������ʵ���ʧ����������ɵ�Mg�����ʵ���Ϊ?mol��
�ο��𰸣�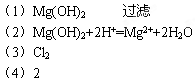
�����������
�����Ѷȣ�һ��