时间:2019-07-03 23:53:44
1、选择题 在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是(?)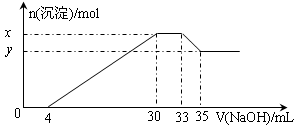
A.原溶液中n(Mg2+)∶n(Al3+)=10∶1
B.原溶液的c(H+)=0.8 mol/L
C.x与y的差值为0.01 mol
D.原溶液中c(Cl-)=0.66mol/L
参考答案:D
本题解析:由图象可知,开始加入氢氧化钠没有沉淀生成,0~4mL发生反应H++OH-=H2O,4mL时H +反应完毕,4~30mL发生反应Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,30mL时沉淀量最大,Mg2+、Al3+沉淀完全,30~33mL沉淀量不变,发生NH4+与氢氧化钠的反应NH4++OH-=NH3·H2O,33~35mL发生Al(OH)3与氢氧化钠的反应Al(OH)3+OH-=AlO2-+2H2O,0~4mL发生H+与氢氧化钠的反应,则H+的物质的量为4mL×10-3L×4mol?L-1=0.016mol,c(H+)=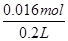 =0.08mol/L,故B错误;由图象可知,x与y的差值即为Al(OH)3的物质的量,由Al(OH)3+NaOH=NaAlO2+2H2O,NaOH的物质的量为(35-33)mL×10-3L×4mol?L-1=0.008mol,即Al(OH)3的物质的量=0.008mol,故C错误;溶液中的阴离子只有Cl―,则加入33mLNaOH溶液时Cl―全部存在于NaCl中,则Cl―的物质的量为33mL×10-3L×4mol?L-1=0.132mol,原溶液中c(Cl―)=
=0.08mol/L,故B错误;由图象可知,x与y的差值即为Al(OH)3的物质的量,由Al(OH)3+NaOH=NaAlO2+2H2O,NaOH的物质的量为(35-33)mL×10-3L×4mol?L-1=0.008mol,即Al(OH)3的物质的量=0.008mol,故C错误;溶液中的阴离子只有Cl―,则加入33mLNaOH溶液时Cl―全部存在于NaCl中,则Cl―的物质的量为33mL×10-3L×4mol?L-1=0.132mol,原溶液中c(Cl―)=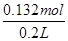 =0.66mol/L,故D正确;由C计算可知n[Al(OH)3]=0.008molmol,则原溶液中n(Al3+)=n[Al(OH)3]=0.008mol,由图可知溶解Al(OH)3消耗氢氧化钠溶液5mL,则沉淀Mg2+、Al3+消耗氢氧化钠溶液26mL,则n(NaOH)=(30-4)mL×10-3L×4mol?L-1=0.104mol,根据氢氧根守恒该阶段有3n[Al(OH)3]+2n[Mg(OH)2]=n(NaOH),则n[Mg(OH)2]=
=0.66mol/L,故D正确;由C计算可知n[Al(OH)3]=0.008molmol,则原溶液中n(Al3+)=n[Al(OH)3]=0.008mol,由图可知溶解Al(OH)3消耗氢氧化钠溶液5mL,则沉淀Mg2+、Al3+消耗氢氧化钠溶液26mL,则n(NaOH)=(30-4)mL×10-3L×4mol?L-1=0.104mol,根据氢氧根守恒该阶段有3n[Al(OH)3]+2n[Mg(OH)2]=n(NaOH),则n[Mg(OH)2]=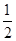 (0.104mol-0.008mol×3)=0.04mol,故原溶液中n(Mg2+)=0.04mol,故原溶液中n(Mg2+):n(Al3+)=5:1,故A错误;
(0.104mol-0.008mol×3)=0.04mol,故原溶液中n(Mg2+)=0.04mol,故原溶液中n(Mg2+):n(Al3+)=5:1,故A错误;
本题难度:一般
2、选择题 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为
[? ]
A.
B.
C.
D.
参考答案:C
本题解析:
本题难度:一般
3、填空题 取等物质的量的MgO和Fe2O3的混合物进行铝热反应,反应的化学方程式为 ,引发铝热反应的实验操作是 。进行铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是 。?
参考答案:2Al+Fe2O3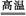 Al2O3+2Fe(2分)
Al2O3+2Fe(2分)
加少量KClO3,插上镁条并将其点燃(2分)
使熔融物易于落下且防止纸漏斗着火(2分)
本题解析:铝热反应只能冶炼活泼性比铝弱的金属,所以只有2Al+Fe2O3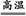 Al2O3+2Fe一个反应发生。铝热反应需要高温,我们可以用镁条引燃。反应产生高温可以使金属熔化,在内层纸漏斗底部剪一小孔并用水润湿可以使熔融物顺利落下并防止纸漏斗着火。
Al2O3+2Fe一个反应发生。铝热反应需要高温,我们可以用镁条引燃。反应产生高温可以使金属熔化,在内层纸漏斗底部剪一小孔并用水润湿可以使熔融物顺利落下并防止纸漏斗着火。
本题难度:简单
4、填空题 化学对人类社会进步和发展的贡 献之一是发现和研制了各种材料,例如金属就是我们生活中不可或缺的重要材料, 根据你学过的有关金属的知识,回答下列问题:
(1)铜钱在我国历史上曾经是一种广泛流通的货币,铜常用于制造货币的原因可能是____(填序号)。
A.铜的熔点不是太高,易于冶炼,铸造成型
B.铜的性质不活泼,不易被腐蚀
C.我国较早地掌握了湿法冶炼铜的技术
D.自然界有大量的游离态的铜 
(2)钢铁制品的使用更为广泛,但是铁制品易生锈,铁锈的主要成分是____(填名称),铁的氧化物常见的还有____、____、(填化学式)。
(3)铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但是该氧化膜易被酸碱破坏,若使氧化铝与氢氧化钠溶液作用,反应的化学方程式为___。
参考答案:(1)A.B.C
(2)氧化铁;FeO ;Fe3O4
(3) Al2O3+ 2NaOH =2NaAlO2+H2O
本题解析:
本题难度:一般
5、选择题 铝土矿的主要成份是
A.氧化铝
B.氧化铁
C.氧化亚铁
D.二氧化硅
参考答案:A
本题解析:铝土矿的主要成份是Al2O3,还含有少量Fe2O3、SiO2。选A
本题难度:简单