时间:2019-07-03 23:49:47
1、填空题 (6分)下列结构图中,代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键。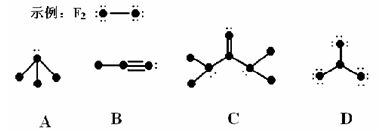
(1) 根据各图表示的结构特点,写出该分子的化学式:
A:________? B:_________? C:________? D:________
(2)与D互为等电子体的化学式??
参考答案:(1) NH3,? HCN,? CO(NH2)2, BF3(各1分)(2)BCl3(2分)
本题解析:(1) A:NH3,B:HCN,? C:CO(NH2)2,D:BF3
(2)与D互为等电子体的化学式:BCl3
本题难度:一般
2、选择题 反应3X(g)+Y(g) 2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的平均速率v为(?)
2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的平均速率v为(?)
A.v(X)=0.05mol・L-1・min-1
B.v(Z)= 0.10mol・L-1・min-1
C.v(Y)=0.10mol・L-1・min-1
D.v(W)=0.05mol・L-1・s-1
参考答案:B
本题解析:先由n(Y)的变化量求5min内Y的变化浓度,再由平均反应速率定义式求Y表示的平均反应速率,最后根据其余反应物和生成物与Y的系数之比等于速率之比求其余物质表示的平均反应速率。依题意,v(Y)=" 0.5mol" ÷2L÷5min="0.05" mol・L-1・min-1,故C错;由于反应3X(g)+Y(g) 2Z(g)+2W(g)中X与Y的系数之比等于速率之比,则v(X)="3" v(Y)=" 0.15" mol・L-1・min-1,故A错;由于反应3X(g)+Y(g)
2Z(g)+2W(g)中X与Y的系数之比等于速率之比,则v(X)="3" v(Y)=" 0.15" mol・L-1・min-1,故A错;由于反应3X(g)+Y(g) 2Z(g)+2W(g)中Z与Y的系数之比等于速率之比,则v(Z)="2" v(Y)=" 0.10" mol・L-1・min-1,故B正确;由于反应3X(g)+Y(g)
2Z(g)+2W(g)中Z与Y的系数之比等于速率之比,则v(Z)="2" v(Y)=" 0.10" mol・L-1・min-1,故B正确;由于反应3X(g)+Y(g) 2Z(g)+2W(g)中W与Y的系数之比等于速率之比,则v(W)="2" v(Y)=" 0.10" mol・L-1・min-1,故D错。
2Z(g)+2W(g)中W与Y的系数之比等于速率之比,则v(W)="2" v(Y)=" 0.10" mol・L-1・min-1,故D错。
本题难度:一般
3、填空题 (12分)中和热的测定是高中重要的定量实验。取0.55 mol/L的NaOH溶液50 mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题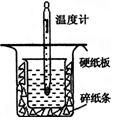
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________ _,除此之外,装置中的一个明显错误是 。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值会_________,(填“偏大”、“偏小”或“不变”)。
(3)实验中改用60 mL 0.50 mol・L-1盐酸跟50 mL 0.55 mol・L-1 NaOH溶液进行反应,与上述实验相比,所求中和热 (填“相等”或“不相等”),简述理由: 。
(4)某实验小组用盐酸和氢氧化钠溶液做了三次实验,每次取溶液各50 mL,并记录下原始数据:
| 实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
| 2 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
| 3 | 25.1 | 25.1 | 25.1 | 27.1 | 2.0 |
参考答案:
(1)环形玻璃搅拌棒;小烧杯口未用硬纸板盖住(或大烧杯内碎纸条塞少了,未将小烧杯垫的足够高)
(2)偏小
(3)相等 因为计算中和热要折算成生成1 mol H2O所放出的热量(与所用酸、碱的用量无关)
(4)HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l);△H=-56.85 KJ/mol.
本题解析:测定中和热应尽量减少热量的损失,且使酸与碱快速充分反应,(1)从装置图可以看出缺少环形玻璃搅拌棒;小烧杯口未用硬纸板盖住(或大烧杯内碎纸条塞少了,未将小烧杯垫的足够高)会造成热量的损失。(2)醋酸是弱酸,电离过程会吸收热量,则测得的中和热数值会偏小;(3)中和热是指中和生成1 mol H2O所放出的热量(与所用酸、碱的用量无关);(4)分析三组数据,舍去第3组数据,取前两组数据的平均值进行计算,反应生成水的物质的量为0.050L×0.5m ol/L=0.025mol,放出的热量为Q=3.4℃×100g×4.18×10-3 kJ/(g・℃)=1.4212KJ,则中和热△H=-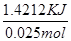 =-56.85 KJ/mol.
=-56.85 KJ/mol.
考点:中和热的测定
本题难度:一般
4、选择题 在298K时,2SO2(g)+O2(g)  2SO3(g) ΔH=-197 kJ・mol-1,在相同的温度下,向密闭真空容器中通入2molSO2和1molO2,达到平衡时放出热量Q1; 向另一个同体积的密闭真空容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2,则下列关系中正确的是
2SO3(g) ΔH=-197 kJ・mol-1,在相同的温度下,向密闭真空容器中通入2molSO2和1molO2,达到平衡时放出热量Q1; 向另一个同体积的密闭真空容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2,则下列关系中正确的是
A.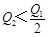
B.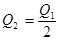
C.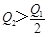
D.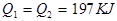
参考答案:A
本题解析:因为二氧化硫与氧气的反应是可能反应,所以反应物不会彻底转化,在相同的温度下,向密闭真空容器中通入2molSO2和1molO2,达到平衡时放出热量Q1,则Q1<197kJ;向另一个同体积的密闭真空容器中通入1molSO2和0.5molO2,若平衡不移动,则放出的热量是Q1的一半,而反应物浓度减少,则平衡逆向进行,所以放出的热量比Q1的一半还少,则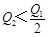 <98.5kJ,答案选A。
<98.5kJ,答案选A。
考点:考查反应物浓度对平衡的影响,可逆反应的理解
本题难度:一般
5、选择题 下列变化中,一定不存在化学能与热能相互转化的是
A.铝热反应
B.金属钝化
C.燃放爆竹
D.干冰气化
参考答案:D
本题解析:只有在化学反应中才存在化学能和热能的相互转化,D是物理变化。所以答案选D
本题难度:简单