时间:2019-07-03 23:49:47
1、选择题 下列物质中,只含有离子键,不含有共价键的是
A.HCl
B.KOH
C.CaCl2
D.CO2
参考答案:C
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属之间容易形成离子键,非金属原子之间形成共价键,因此A中含有极性键,B中含有离子键和极性键,C中含有离子键,D中极性键。答案选C。
本题难度:简单
2、选择题 已知H2(g)+Br2(l)="2HBr(g)" △H= -72kJ・mol-1,蒸发1mol Br2(l)需要吸收的能量为30kJ,断裂1mol气态H2、Br2、HBr分子内的化学键分别需要吸收的能量为436kJ、akJ、369kJ,则数据a为
A.404
B.260
C.230
D.200
参考答案:D
本题解析:断开化学键要吸收能量,形成化学键要放出热量,Br2(g)=Br2(l) △H1=-30kJ/mol,H2(g)+Br2(l)=2HBr(g)△H2=-72kJ/mol,H2(g)+Br2(g)=2HBr(g)△H=△H1+△H2即(436+a)-369*2=-102解得a=200;答案选D。
考点:反应热与键能的关系
本题难度:一般
3、填空题 (11分)测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示.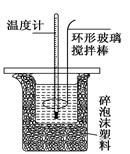
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol): ;
(2) 装置图中碎泡沫塑料所起作用为: ;
(3) ①取50 mL NaOH溶液和30 mL硫酸溶液进行实验,
实验数据如下表.请填写下表中的空白:
| 温度 实验次数 | 起始温度T1/℃ | 终止温度T2/℃ | 温度差平均值(T2-T1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
参考答案:(1)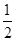 H2SO4(aq)+NaOH(aq)===
H2SO4(aq)+NaOH(aq)===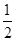 Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol (2)保温、隔热,防止
Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol (2)保温、隔热,防止
热量损失 (3)①4.0 ②a、c、d
本题解析:
试题解析:(1)稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,稀硫酸和氢氧化钠稀溶液分别是强酸、强碱,则反应的热化学方程式为:NaOH(aq)+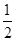 H2SO4(aq)
H2SO4(aq)
本题难度:一般
4、选择题 下列过程中△H小于零的是( )
A.氯酸钾分解制氧气
B.氯化铵分解得氨气
C.碳酸钙分解得二氧化碳
D.实验室制备氢气
参考答案:D
本题解析:考查常见的放热反应和吸热反应。一般金属和水或酸反应,酸碱中和反应,一切燃烧,大多数化合反应和置换反应,缓慢氧化反应如生锈等是放热反应。大多数分解反应,铵盐和碱反应,碳、氢气或CO作还原剂的反应等是吸热反应。△H小于零,说明该反应是放热反应,所以选项D正确,其余都是吸热反应,答案选D。
本题难度:一般
5、选择题 下列变化中不包含旧键断裂和新键形成的是
A.碘晶体的升华
B.氢气在氯气中燃烧
C.过氧化钠露置空气中
D.用湿润的淀粉碘化钾试纸检验氯气
参考答案:A
本题解析:碘升华是物理变化,化学键不变;氢气在氯气中燃烧、过氧化钠露置空气中、用湿润的淀粉碘化钾试纸检验氯气均是化学变化,既有旧键断裂,也有新键形成,所以答案选A。
点评:该题是基础性试题的考查,也是高考中的常见题型和考点。试题基础性强,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确常见变化的实质,然后灵活运用即可。
本题难度:一般