时间:2019-07-03 23:34:34
1、选择题 镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:xMg+Mo3S4 MgxMo3S4;在镁原电池放电时,下列说法错误的是
MgxMo3S4;在镁原电池放电时,下列说法错误的是
[? ]
A.Mg2+向正极迁移
B.正极反应为:Mo3S4+2xe-= Mo3S42x-
C.Mo3S4发生氧化反应
D.负极反应为:xMg-2xe-= xMg2+
2、选择题 由于具有超低耗电量、寿命长的特点,LED 产品越来越受人们的欢迎。如图是氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是 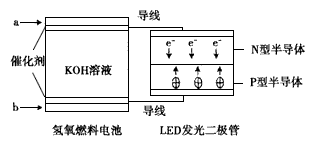
[? ]
A.a处通入的气体是氧气,b处通入的气体是氢气
B.该装置中只涉及两种形式的能量转化
C.电池的正极反应式为O2+2H2O+4e-=4OH-
D.P型半导体连接的是电池的负极
3、选择题 下图为氢氧燃料电池的原理示意图,按照此图的提示,下列叙述不正确的是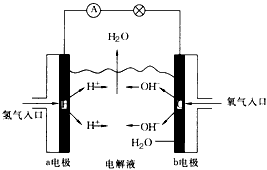
[? ]
A.a电极是负极
B.b电极的电极反应式为:4OH- -4e-=2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储存在电池内的新型发电装置
4、选择题 将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。已知,通入 CH4的一极,其电极反应式是CH4+10OH--8e-===CO32-+7H2O;通入O2的另一极,其电极反应式是2O2+4H2O+8e-===8OH-。下列叙述不正确的是
A.正极发生还原反应
B.通入CH4的电极为负极
C.该电池使用一段时间后应补充KOH
D.燃料电池工作时,溶液中的OH-向正极移动
5、填空题 请回答氯碱的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k= (要求计算表达式和结果);
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。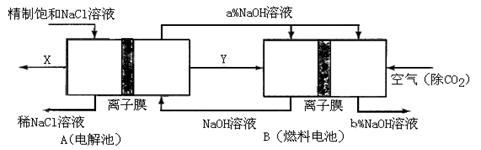
①图中X.Y分别是 、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
②分别写出燃料电池B中正极、负极上发生的电极反应
正极: ;
负极: ;