时间:2019-07-03 23:28:34
1、填空题 能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇: ?
反应I:?CO(g)?+?2H2(g)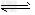 CH3OH(g)?ΔH1 ?
CH3OH(g)?ΔH1 ?
反应II:CO2(g)?+?3H2(g)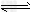 CH3OH(g)?+?H2O(g)?ΔH2
CH3OH(g)?+?H2O(g)?ΔH2
①在以上制备甲醇的两个反应中:反应I优于反应II,原因为___________。?
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。? 
I、在一密闭容器中发生反应Ⅰ并达到平衡后,保持其他条件不变,对容器升温,此反应的化学反应平衡应__________移动(填“正向”、“逆向”、“不”)?。
II、某温度下,将1mol?CO和4mol?H2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=?0.1?mol/L,则CO的转化率为___________,此时的温度______________250℃(填“>”、“<”、“=”)
(2)已知在常温常压下:
①?2CH3OH(l)?+?3O2(g)?=?2CO2(g)?+?4H2O(g)?ΔH?=?-1275.6?kJ/mol
②?2CO?(g)+?O2(g)?=?2CO2(g)?ΔH?=?-566.0?kJ/mol
③?H2O(g)?=?H2O(l)?ΔH?=?-44.0?kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:__________________
(3)某同学依据甲醇燃烧的反应原理,设计如图所示的电池装置,工作一段时间后,测得溶液的pH将____________(填“升高”、“降低”、“不变”),该燃料电池负极反应的离子方程式为:___________________。? 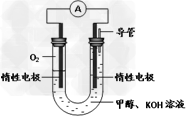
2、选择题 铜锌原电池(如图)工作时,下列叙述正确的是 
[? ]
A.正极反应为:Zn - 2e- = Zn2+
B.电池反应为:Zn + Cu2+ = Zn2+ + Cu
C.Cu2+氧化性较强,作为负极
D.盐桥中的K+移向ZnSO4溶液
3、选择题 如图把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池。某实验兴趣小组做完实验后,在读书卡上的记录如下所示,则卡片上的描述合理的是(?)
卡片号:2013.4
实验后的记录:
①Cu为阳极,Zn为阴极?②Cu极上有气泡产生
③SO42-向Cu极移动?④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子流向是:Cu  Zn
Zn
⑥正极反应式:Cu + 2e- = Cu2+
A.①②③
B.②④
C.④⑤⑥
D.③④⑤
4、填空题 新型锂离子电池材料Li2 MSiO4(M为Fe,Co,Mn,Cu等)是一种发展潜力很大的电池电极材料。工业制备Li2 MSiO4有两种方法:
方法一:固相法,2Li2SiO3+ FeSO4 Li2FeSiO4 +Li2SO4 +SiO2
Li2FeSiO4 +Li2SO4 +SiO2
方法二:溶胶―凝胶法,
 Li2FeSiO4
Li2FeSiO4
(1)固相法中制备Li2 FeSiO4过程采用惰性气体气氛,其原因是 ;
(2)溶胶―凝胶法中,检查溶液中有胶体生成的方法是 ;生产中生成Imol Li2FeSiO4整个过程转移电子物质的量为 mol;
(3)以Li2 FeSiO4和嵌有Li的石墨为电极材料,含锂的导电固体作电解质,构成电池的总反应式为:Li+ LiFeSiO4 Li2FeSiO4则该电池的负极是____ ;充电时,阳极反应的电极反应式为 ;
Li2FeSiO4则该电池的负极是____ ;充电时,阳极反应的电极反应式为 ;
(4)使用(3)组装的电池必须先____ 。
5、选择题 下列叙述中,金属甲的活动性一定比金属乙的活动性强的是
[? ]
A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多
B.同价态的阳离子,甲比乙的氧化性强
C.甲能跟稀盐酸反应放出氢气而乙不能
D.将甲、乙作电极组成原电池时,甲是正极