Кұјд:2019-07-03 23:21:21
1ЎўјЖЛгМв (10·Ц)(1)12.4 g Na2Xә¬УР0.4 mol NaЈ«Ј¬Na2XөДДҰ¶ыЦКБҝОӘ_____Ј¬ЖдПа¶Ф·ЦЧУЦКБҝОӘ______Ј¬XөДПа¶ФФӯЧУЦКБҝОӘ________Ј¬ёГОпЦКөД»ҜС§КҪОӘ________ЎЈ
(2)ПаН¬ЧҙҝцПВЈ¬Т»¶ЁМе»эөДЖшМ¬Зв»ҜОпHmXөДЦКБҝКЗөИМе»эNH3өД2ұ¶ЎЈФтXөДПа¶ФФӯЧУЦКБҝОӘ________ЎЈЈЁУГә¬mөДҙъКэКҪұнКҫЈ©
(3)aёцXФӯЧУөДЧЬЦКБҝОӘb gЈ¬ФтXөДПа¶ФФӯЧУЦКБҝҝЙұнКҫОӘ________ЎЈ
(4)20 g AОпЦКәН14 g BОпЦКНкИ«·ҙУҰЈ¬ЙъіЙ8.8 g CОпЦКЎў3.6 g DОпЦКәН0.2 mol EОпЦКЈ¬ФтEОпЦКөДДҰ¶ыЦКБҝОӘ________ЎЈ
(5)483 g Na2SO4ЎӨ10H2OЦРЛщә¬өДNa+өДОпЦКөДБҝКЗ molЈ¬SO42ЎӘөДОпЦКөДБҝКЗ molЈ¬Лщә¬OФӯЧУөДКэДҝКЗ ёцЎЈ
ІОҝјҙр°ёЈәЈЁ10·ЦЈ¬ГҝҝХ1·ЦЈ©(1)62g/mol 62 16 Na2O (2)34-m (3)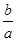 NA
NA
(4)108g/mol (5)3 1.5 21NA
ұҫМвҪвОцЈәҝјІйОпЦКөДБҝөДУР№ШјЖЛгЎЈ
ЈЁ1Ј©12.4 g Na2Xә¬УР0.4 mol NaЈ«Ј¬Фт»ҜәПОпөДОпЦКөДБҝКЗ0.2molЈ¬ЛщТФёГ»ҜәПОпөДДҰ¶ыЦКБҝКЗ12.4gЎВ0.2molЈҪ62g/molЈ»ЖдПа¶Ф·ЦЧУЦКБҝКЗ62Ј¬XөДПа¶Ф·ЦЧУЦКБҝКЗ62Јӯ23ЎБ2=16Ј¬ЛщТФXКЗOЈ¬ФтёГ»ҜәПОпКЗNa2OЎЈ
ЈЁ2Ј©ПаН¬ЧҙҝцПВЈ¬Т»¶ЁМе»эөДЖшМ¬Зв»ҜОпHmXөДЦКБҝКЗөИМе»эNH3өД2ұ¶Ј¬Фт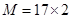 Ј¬ҪвөГMЈҪ34Ј¬ЛщТФXФӯЧУөДПа¶ФФӯЧУЦКБҝКЗ34ЈӯmЎЈ
Ј¬ҪвөГMЈҪ34Ј¬ЛщТФXФӯЧУөДПа¶ФФӯЧУЦКБҝКЗ34ЈӯmЎЈ
ЈЁ3Ј©ёщҫЭMЈҪm/nәН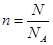 ҝЙЦӘЈ¬XөДПа¶ФФӯЧУЦКБҝҝЙұнКҫОӘ
ҝЙЦӘЈ¬XөДПа¶ФФӯЧУЦКБҝҝЙұнКҫОӘ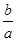 NAЎЈ
NAЎЈ
ЈЁ4Ј©ёщҫЭЦКБҝКШәг¶ЁВЙҝЙЦӘЈ¬EОпЦКөДЦКБҝКЗ20gЈ«14gЈӯ8.8gЈӯ3.6gЈҪ21.6gЈ¬ЛщТФEөДДҰ¶ыЦКБҝКЗ21.6gЎВ0.2molЈҪ108g/molЎЈ
ЈЁ5Ј©483 g Na2SO4ЎӨ10H2OөДОпЦКөДБҝКЗ483gЎВ322g/molЈҪ1.5molЈ¬ФтДЖАлЧУөДОпЦКөДБҝКЗ3.0molЈ¬SO42ЈӯөДОпЦКөДБҝКЗ1.5molЎЈСхФӯЧУөДОпЦКөДБҝКЗ14ЎБ1.5molЈҪ21molЈ¬ФӯЧУКэёцКэКЗ21NAЎЈ
ұҫМвДС¶ИЈәТ»°г
2ЎўСЎФсМв ПВБРЛө·ЁІ»ХэИ·өДКЗ
AЈ®6.02ЎБ1023ҫНКЗ°ў·ьјУөВВЮіЈКэ
BЈ®0.012 kg C12ә¬УРөДМјФӯЧУКэҫНКЗ°ў·ьјУөВВЮіЈКэөДЦө
CЈ®ә¬УР°ў·ьјУөВВЮіЈКэёцБЈЧУөДОпЦКөДБҝКЗ1 mol
DЈ®1 mol NH3Лщә¬ФӯЧУКэФјКЗ2.408ЎБ1024
ІОҝјҙр°ёЈәA
ұҫМвҪвОцЈә0.012kg12CЦРЛщә¬өДМјФӯЧУөДёцКэОӘ°ў·ьјУөВВЮіЈКэЈ¬КэЦөЙПФјОӘ6.02ЎБ1023Ј¬AҙнОуЈ¬BХэИ·Ј»ә¬УР°ў·ьјУөВВЮіЈКэёцБЈЧУөДОпЦКөДБҝКЗ1 molЈ¬CХэИ·Ј»1 mol NH3Лщә¬·ЦЧУКэОӘ6.02ЎБ1023Ј¬Т»ёц°ұЖш·ЦЧУЦРә¬УР4ёцФӯЧУЈ¬№КФӯЧУКэФјОӘ2.408ЎБ1024Ј¬DХэИ·Ј¬ҙр°ёСЎA.
ҝјөгЈә°ў·ьЩӨөВВЮіЈКэ
ұҫМвДС¶ИЈәТ»°г
3ЎўСЎФсМв Иф20 gГЬ¶ИОӘҰС g/cm3өДCa(NO3)2ИЬТәАпә¬1 g Ca2Ј«Ј¬ФтNO3ЎӘөДОпЦКөДБҝЕЁ¶ИКЗ(ЎЎЎЎ)
AЈ®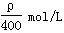
BЈ®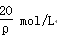
CЈ®2.5 ҰСmol/L
DЈ®1.25 ҰСmol/L
ІОҝјҙр°ёЈәC
ұҫМвҪвОцЈә20ҝЛГЬ¶ИОӘҰСg/cm3өДПхЛбёЖИЬТәөДМе»эОӘ20g/ҰСg/cm3=(20/ҰС)ЎБ10-3LЈ¬
1ҝЛCa2+өДОпЦКөДБҝОӘ1g/40(g/mol) =0.025molЈ¬
ФтCa2+өДОпЦКөДБҝЕЁ¶ИОӘ0.025mol/[((20/ҰС) ЎБ10-3L) =1.25ҰСmol/LЈ¬
УЙПхЛбёЖөД»ҜС§КҪCaЈЁNO3Ј©2Ј¬
ФтNO3-АлЧУөДЕЁ¶ИОӘ1.25dmol/LЎБ2=2.5mol/LЈ¬
№КСЎCЎЈ
өгЖАЈәұҫМвҝјІйОпЦКөДБҝЕЁ¶ИөДјЖЛгЈ¬ГчИ·ёЖАлЧУөДОпЦКөДБҝөДјЖЛгКЗҪвҙрөД№ШјьЈ¬ёЖАлЧУөДЦКБҝУлёЖФӯЧУөДЦКБҝҝЙҪьЛЖПаөИЈ¬әцВФөзЧУөДЦКБҝАҙ·ЦОцҪвҙрЎЈ
ұҫМвДС¶ИЈәТ»°г
4ЎўСЎФсМв УГNaOH№ММеЕдЦЖТ»¶ЁОпЦКөДБҝЕЁ¶ИөДИЬТәКұЈ¬ұШРлУГөҪөДТЗЖчКЗЈЁЎЎЎЎЈ©
AЈ®·ЦТәВ©¶·
BЈ®ЙХЖҝ
CЈ®ИЭБҝЖҝ
DЈ®Хф·ўГу
ІОҝјҙр°ёЈәёщҫЭЕдЦЖТ»¶ЁОпЦКөДБҝЕЁ¶ИөДЗвСх»ҜДЖИЬТәөДІҪЦиҝЙЦӘЈ¬ЕдЦЖ№эіМЦРК№УГөДТЗЖчУРЈәНРЕММмЖҪЎўТ©іЧЎўЙХұӯЎўІЈБ§°фЎўИЭБҝЖҝЎўҪәН·өО№ЬөИЈ¬ЛщТФСЎПоЦРұШРлК№УГөДТЗЖчОӘИЭБҝЖҝЈ¬¶ш·ЦТәВ©¶·ЎўЙХЖҝәНХф·ўГуЈ¬ФЪЕдЦЖЦРІ»»бУГөҪЈ¬
№КСЎCЈ®
ұҫМвҪвОцЈә
ұҫМвДС¶ИЈәјтөҘ
5ЎўСЎФсМв 100 mL 0.3mol/L Na2SO4ИЬТәәН50mL 0.2mol/LAl2(SO4)3ИЬТә»мәПәуЈ¬ИЬТәЦРSO42-АлЧУөДОпЦКөДБҝЕЁ¶ИОӘ(ЎЎ )
AЈ®0.20molЈҜL
BЈ®0.25molЈҜL
CЈ®0.40molЈҜL
DЈ®0.50molЈҜL
ІОҝјҙр°ёЈәC
ұҫМвҪвОцЈәПЎИЬТә»мәПКұҝЙИПОӘЧЬМе»эОӘБҪИЬТәМе»эЦ®әНЎЈПИЗуіцNa2SO4әНAl2(SO4)3ОпЦКөДБҝЈ¬ФЩЗуSO42-АлЧУЕЁ¶ИЎЈ
ұҫМвДС¶ИЈәјтөҘ