时间:2019-06-28 22:56:20
1、实验题 50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: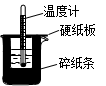
(1)从实验装置看,图中尚缺少的一种玻璃用品是_______________。?
(2)烧杯间填满碎纸条的作用是_________________________。
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量__________(填“相等”或“不相等”),中和热__________(填“相等”或“不相等”),理由是__________________________________。
(4)用50mL0.50mol/L的醋酸代替盐酸溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会____________。(填“偏大”、“偏小”或“无影响”)。
(5)完整地做一次这样的实验,需测定______次温度。
(6)大烧杯上如不盖硬纸板,求得的中和热数值?(填“偏大”、“偏小”或“无影响”)
参考答案:(1)环形玻璃搅拌棒?(2)减少实验过程中热量损失?
(3)不相等?相等?因为中和热是指在稀溶液中,酸跟碱发生中和反应生成1molH2O所放出的能量,与酸碱用量无关?⑷偏小(5)3?(6)偏小
本题解析:考查中和热的测定及误差分析等
(1)在实验过程中,微粒使溶液混合均匀,需要搅拌,因此好缺少的仪器是环形玻璃搅拌棒。
(2)在实验过程中,需要尽可能的减少热量的损失,所以烧杯间填满碎纸条的作用是减少实验过程中热量损失。
(3)由于中和热是指在稀溶液中,酸跟碱发生中和反应生成1molH2O所放出的能量,与酸碱用量无关。所以改变酸或碱的用量,反应中放出的热量可以改变,但中和热是不变的。
(4)醋酸是弱电解质,存在电离平衡。而电离是吸热的,所以测定的数值会偏小。
(5)为了减小实验误差,应该至少测定3次温度,然后求其平均值。
(6)大烧杯上如不盖硬纸板,则热量会损失,因此得的中和热数值偏小。
本题难度:一般
2、填空题 (6分)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵,⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)?。
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)?
(3)将②和③等体积混合后,混合液中各离子浓度由大到小的顺序是
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”) ?25℃。在t℃时将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= ?。
(5)若室温时pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则该氨水的电离度可表示为 ?
参考答案:(1)④②③①?(2)⑥⑦④⑤⑧?(3)c(Na+)> c(CH3COO-) >c(OH-)>c(H+)
(4)>;9:2? (5) 10(a+b-12)%
本题解析:考查弱电解质的电离以及pH的有关计算。
(1)水在溶液中存在电离平衡H2O H++OH-,所以酸或碱均是抑制水的电离,如果氢离子浓度和OH―如果相同,对水的电离抑制程度就相同的。盐的水解可以促进水的电离。硫酸是二元强酸,醋酸是一元弱酸,氢氧化钠是一元强碱,氯化铵溶于水存在水解平衡,所以由水电离出的H+浓度由大到小的顺序是④②③①。
H++OH-,所以酸或碱均是抑制水的电离,如果氢离子浓度和OH―如果相同,对水的电离抑制程度就相同的。盐的水解可以促进水的电离。硫酸是二元强酸,醋酸是一元弱酸,氢氧化钠是一元强碱,氯化铵溶于水存在水解平衡,所以由水电离出的H+浓度由大到小的顺序是④②③①。
(2)氨水是弱碱部分电离,所以NH4+浓度最小。另外四种属于铵盐,NH4+水解显酸性,⑦中能电离出大量的氢离子,抑制其水解,⑤中阳离子和阴离子均水解,相互促进。所以溶液中NH4+浓度由大到小的顺序是⑥⑦④⑤⑧。
(3)②和③等体积混合后,二者恰好反应生成醋酸钠,醋酸钠水解显碱性,所以混合液中各离子浓度由大到小的顺序是c(Na+)> c(CH3COO-) >c(OH-)>c(H+)。
(4)电离是吸热的,所以升高温度,促进水的电离,离子积常数增大。所得混合溶液的pH=2,说明硫酸是过量的。pH=11的NaOH溶液,则O 91eXAm.orgH―的浓度为0.01mol/L,硫酸中氢离子是0.1mol/L,所以有 ,解得a∶b=9∶2。
,解得a∶b=9∶2。
(5)pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则氨水的浓度和元素的浓度相等,都是10-bmol/L,根据氨水的电离方程式和pH可计算氨水中已电离的一水合氨的浓度为10a-14mol/L,所以室温下氨水的电离度为 。
。
本题难度:一般
3、选择题 已知热化学方程式C2H2 (g)+5/2O2 (g)=2CO2 (g)+H2O(g);△H="-1256" kJ/mol,下列说法正确的是
A.乙炔的燃烧热为1256kJ/mol
B.若生成2mol 液态水,则放出的热量小于2512kJ
C.若形成4mol碳氧共用电子对,则放出的热量为2512kJ
D.若转移10mol电子,则消耗2.5molO2
参考答案:D
本题解析:略
本题难度:一般
4、选择题 下列说法正确的是
A.pH=5的盐酸,再加水冲稀1000倍,溶液的pH=8
B.给稀醋酸溶液适当加热,溶液pH值增大
C.pH=1的盐酸中c(H+)是pH=3的盐酸的100倍
D.在Na2CO3溶液中,C(Na+) :C(CO32-)=2∶1
参考答案:C
本题解析:A:酸性溶液稀释后pH只能无限接近7,但不可能超过7,不正确
B:适当加热可促进醋酸的电离平衡正向移动,酸性增强,pH减小,不正确
C:正确
D:由于CO32-部分水解,故C(Na+) :C(CO32-)>2∶1,排除
本题难度:一般
5、选择题 下列水溶液一定呈中性的是
A.pH=7的溶液
B.c(H+)=1.0×10-7mol·L-1的溶液
C.c(H+) =c(OH-)
D.pH=3的与pH=11的碱等体积混合后的溶液
参考答案:C
本题解析:溶液的酸碱性是由c(H+)与c(OH-)的相对大小决定的
本题难度:简单