ʱ��:2019-06-28 22:47:27
1������� ��14�֣���1����һ���¶��£���1L����̶����ܱ������м���1mol A��g����������Ӧ2A��g�� B��g��+C��g����B�����ʵ�����ʱ��ı仯��ͼ��ʾ�� 0��2min�ڵ�ƽ����Ӧ����v(A)= ?. ��ͬ�¶��£�����ʼ����A��g�������ʵ�����ԭ����2������ƽ��ʱ?��ԭ����2����
B��g��+C��g����B�����ʵ�����ʱ��ı仯��ͼ��ʾ�� 0��2min�ڵ�ƽ����Ӧ����v(A)= ?. ��ͬ�¶��£�����ʼ����A��g�������ʵ�����ԭ����2������ƽ��ʱ?��ԭ����2����
a.ƽ�ⳣ��? b. A��ƽ��Ũ��?
c.ƽ��ʱ���������ܶ�? d.ƽ��ʱB���������
��2��ʵ������Zn��ϡ������ȡH2����Ӧʱ��Һ��ˮ�ĵ���ƽ��??�ƶ�����������ҡ������������������������Լ��е�??������H2�����ʽ�����
a.NaNO3? b.CuSO4 ?
c.Na2SO4?d.NaHSO3?
e.? CH3COOH?
��3���ö��Ե缫���Cu(NO3)2��Һһ��ʱ�����a mol ��Cu(OH)2��ʹ��Һ�ָ�ԭ״�����������ת�Ƶĵ�����ĿΪ_____________
��4����֪��2Zn��s��+O2��g��=2ZnO��s��?��H=-701.0kJ��mol-1
2Hg��l��+O2��g��=2HgO��s��?��H=-181.6kJ��mol-1
��ӦZn��s��+ HgO��s��=ZnO��s��+ Hg��l��?��H=_____________
��5����֪25��ʱ��Ksp[Cu(OH)2]��2��10��20,Ҫʹ0.2 mol��L��1 CuSO4��Һ��Cu2��������Ϊ��ȫ��ʹCu2��Ũ�Ƚ���ԭ����ǧ��֮һ������Ӧ����Һ�����NaOH��Һ��ʹ��Һ��pHΪ��������������
�ο��𰸣�����14�֣���1��0.1mol/(L��min) �� b c ��2������?�� b
��3��4a NA?��4����259��7 kJ��mol-1?��5��6
�����������1����0��2min��B������0.1mol������ݷ�ӦʽA������0.2mol��������Ӧ������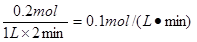 �����ڷ�Ӧǰ��������䣬��������ʼ����A��g�������ʵ�����ԭ����2������ƽ��ʱA��ƽ��Ũ�Ⱥ�ƽ��ʱ���������ܶȶ���ԭ����2����ac���Dz���ģ���ѡbc��
�����ڷ�Ӧǰ��������䣬��������ʼ����A��g�������ʵ�����ԭ����2������ƽ��ʱA��ƽ��Ũ�Ⱥ�ƽ��ʱ���������ܶȶ���ԭ����2����ac���Dz���ģ���ѡbc��
��2��п��ϡ���ᷴӦ��������������Һ�������ӵ�Ũ�Ƚ��ͣ�����ˮ�ĵ���ƽ��������Ӧ�����ƶ����������ƶ���b���Թ���ͭпԭ��أ��ӿ췴Ӧ���ʡ�a�в��ٲ���������b��Ӱ�죬d�����������ӣ����Ʒ�Ӧ���ʡ����������ᣬ�������������ӵ�Ũ�ȣ���ѡb��
��3����a mol ��Cu(OH)2��ʹ��Һ�ָ�ԭ״��˵���ڷ�Ӧ������������������������ʼ����OH���ŵ����������a mol Cu(OH)2�к���2amol��ԭ�ӣ����Է�Ӧ��ת�Ƶĵ�����2amol��2��4amol��
��4�������˹���ɵ�Ӧ�ã����٣��ڣ���2���õ�Zn��s��+ HgO��s��=ZnO��s��+ Hg��l�������Է�Ӧ���ǣ���701.0kJ��mol-1��181.6kJ��mol-1����2����259��7 kJ��mol-1.
��5�������ܶȻ������ı���ʽ��֪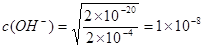 ����������Ũ����
����������Ũ����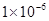 ������pH��6.
������pH��6.
�����Ѷȣ�һ��
2��ʵ���� (15��)�Ҵ�����Ҫ���л�����ԭ�ϣ�������ϩֱ��ˮ�Ϸ�����ˮ�Ϸ��������ش��������⣺
��1�����ˮ�Ϸ���ָ�Ƚ���ϩ��Ũ���ᷴӦ��������������(C2H5OSO3H)����ˮ�������Ҵ���д����Ӧ�ķ�Ӧ�Ļ�ѧ����ʽ?
��2����֪��
�״���ˮ��Ӧ��2CH3OH(g)��CH3OCH3(g)��H2O(g)?��H1����23.9KJ��mol��1
�״���ϩ����Ӧ��2CH3OH(g)��C2H4 (g)��2H2O(g)? ��H2����29.1KJ��mol��1
�Ҵ��칹����Ӧ��CH3CH2OH(g)��CH3OCH3(g))? ��H3��+50.7KJ��mol��1
����ϩ����ֱ��ˮ�Ϸ�ӦC2H4 (g)��H2O(g)��C2H5OH(g)��?��H��? KJ��mol��1
����ˮ�Ϸ���ȣ�����ֱ��ˮ�Ϸ����ŵ��ǣ�?��
��3����ͼΪ����ֱ��ˮ�Ϸ�����ϩ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ(����n(H2O)�Un(C2H4)=1�U1)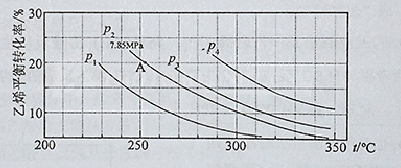
����ʽ������ϩˮ�����Ҵ���Ӧ��ͼ��A���ƽ�ⳣ��K��?(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�������)
��ͼ��ѹǿP1��P2��P3��P4�Ĵ�С˳��Ϊ��?�������ǣ�?
������ֱ��ˮ�Ϸ������õĹ�������Ϊ������/������Ϊ��������Ӧ�¶�290 �棬ѹǿ6��9MPa��n(H2O)�Un(C2H4)=0��6�U1����ϩ��ת����Ϊ5�G����Ҫ��һ�������ϩ��ת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Բ�ȡ�Ĵ�ʩ�У�??��?��
�ο��𰸣���1��C2H4+H2SO4= C2H5OSO3H; C2H5OSO3H��H2O=C2H5OH+ H2SO4;
(2) -45.5?��ȾС����ʴ��С�ȣ���3����K=0.07(MPa)-1; ��P1< P2< P3< P4;��Ӧ���������٣���ͬ�¶��£�ѹǿ���ߣ���ϩת������ߣ�? �۽������Ҵ�Һ��ת��ȥ������n(H2O):n(C2H4)�ıȡ�
�����������1����������ɵ���ϩ��Ũ���ᷴӦ��������������C2H5OSO3H�ķ���ʽ��C2H4+H2SO4= C2H5OSO3H; C2H5OSO3H��H2O=C2H5OH+ H2SO4����2���٣��ڣ��ۣ������ɵ�C2H4 (g)��H2O(g)��C2H5OH(g)����H������23.9+29.1��50.7��KJ/mol=��45.5 KJ/mol������ˮ�Ϸ���ȣ�����ֱ��ˮ�Ϸ����ŵ�����ȾС����ʴ��С�ȣ���3������ϩˮ�����Ҵ���Ӧ��ͼ��A���ƽ�ⳣ��K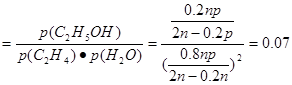 (MPa)-1; ������ͬ���¶���������ϩ��ƽ��ת������P1< P2< P3< P4;�ɷ���ʽC2H4 (g)��H2O(g)��C2H5OH(g)��֪�÷�Ӧ������Ӧ�����������С�ķ�Ӧ����������ѹǿ��ƽ�������ƶ�����ϩ��ת������ߣ����ѹǿ��ϵ�ǣ�P1< P2< P3< P4; ����Ҫ��һ�������ϩ��ת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Բ�ȡ�Ĵ�ʩ�иı����ʵ�Ũ�ȣ����ƽ����ϵ�н������Ҵ������ȥ��������ˮ������Ũ�ȣ��ı���ߵ����ʵ����ıȵȵȡ�
(MPa)-1; ������ͬ���¶���������ϩ��ƽ��ת������P1< P2< P3< P4;�ɷ���ʽC2H4 (g)��H2O(g)��C2H5OH(g)��֪�÷�Ӧ������Ӧ�����������С�ķ�Ӧ����������ѹǿ��ƽ�������ƶ�����ϩ��ת������ߣ����ѹǿ��ϵ�ǣ�P1< P2< P3< P4; ����Ҫ��һ�������ϩ��ת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Բ�ȡ�Ĵ�ʩ�иı����ʵ�Ũ�ȣ����ƽ����ϵ�н������Ҵ������ȥ��������ˮ������Ũ�ȣ��ı���ߵ����ʵ����ıȵȵȡ�
�����Ѷȣ�һ��
3��ѡ���� ������ɱ���ܱ������У���ӦmA��g����nB��s�� pC��g���ﵽƽ���ѹ�����������������A��ת������֮���͡�����˵������ȷ����
pC��g���ﵽƽ���ѹ�����������������A��ת������֮���͡�����˵������ȷ����
A����m��n���ض�С��p
B����m��n���ض�����p
C��m�ض�С��p
D��n�ض�����p
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
4�������� ��8�֣��������ʵ�����A��B�����1 L���ܱ������У��������·�Ӧ
3A(g)��B(g)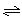 ?xC(g)��2D(g)����5 min���D��Ũ��Ϊ0.5 mol/L��c(A)��c(B)��3��5��C��ƽ����Ӧ����Ϊ0.1 mol/(L��min)����
?xC(g)��2D(g)����5 min���D��Ũ��Ϊ0.5 mol/L��c(A)��c(B)��3��5��C��ƽ����Ӧ����Ϊ0.1 mol/(L��min)����
(1)��ʱA��Ũ��c(A)��________mol/L����Ӧ��ʼǰ�����е�A��B�����ʵ�����n(A)��n(B)��________mol��
(2)B��ƽ����Ӧ����v(B)��________mol/(L��min)��?
(3)x��ֵΪ________��
�ο��𰸣�(1)0.75��1.5? (2)0.05? (3) 2?��ÿ��2�֣�
���������������淴Ӧ���йؼ��㡣
��1��C��ƽ����Ӧ������0.1mol/(L��min)����C��Ũ����0.5mol/L�����Ը��ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪x��2������Ϊ��Ӧ����֮������Ӧ�Ļ�ѧ������֮�ȣ�����B�ķ�Ӧ������0.1mol/(L��min)��2��0.05mol/(L��min)��
��2��? 3A��g��+B(g) 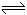 2C(g)+2D(g)
2C(g)+2D(g)
��ʼ����mol��? n? n? 0? 0
ת������mol��? 0.5? 0.25? 0.5? 0.5
ƽ������mol��? n��0.75? n��0.25? 0.5? 0.5
������n��0.75���U��n��0.25���� 3:5
���n��1.5mol������A��Ũ����0.75mol��1L��0.75mol/L
�����Ѷȣ�һ��
5��ѡ���� ����ƽ�ⳣ��������˵������ȷ����
A��ƽ�ⳣ�����¶ȵĸı���ı�
B��ʹ�ô������ܸı�ƽ�ⳣ��
C��ƽ�ⳣ�����淴Ӧ���������Ũ�ȵĸı���ı�
D������ѹǿ��ʹƽ��������Ӧ������У���ƽ�ⳣ������
�ο��𰸣�D
���������ƽ�ⳣ��ֻ���¶��йأ��¶ȸı䣬ƽ�ⳣ��һ���ı䣬�뷴Ӧ��������Ũ���أ�����A��C��ȷ������ֻ�ı䷴Ӧ���ʣ�����ı�ƽ�⣬����ƽ�ⳣ�����䣬B����ƽ�������ƶ���ƽ�ⳣ������D��ȷ����ѡD��
�����Ѷȣ���