时间:2019-06-28 22:06:37
1、选择题 在体积可变的密闭容器中,反应mA(g)+nB(s) pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法中正确的是
pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法中正确的是
A.(m+n)必定小于p
B.(m+n)必定大于p
C.m必定小于p
D.n必定大于p
参考答案:C
本题解析:略
本题难度:一般
2、选择题 现有X(g)+Y(g) 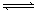 2Z(g);正反应放热。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据下图回答:从t2→t3的曲线变化是由哪种条件引起的
2Z(g);正反应放热。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据下图回答:从t2→t3的曲线变化是由哪种条件引起的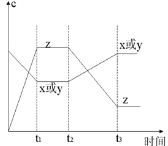
A.增大X或Y的浓度
B.增大压强
C.增大Z的浓度
D.升高温度
参考答案:D
本题解析:根据图像可知,从t2→t3时,生成物Z的浓度逐渐降低,而反应物的浓度逐渐增大,这说明平衡向逆反应方向移动,所以根据正反应是体积增大的、吸热放热可逆反应可知,改变的条件应该是升高温度,答案选D。
点评:在分析有关图像时应该注意:一、ν-t 图像或 c-t 图像:1.ν-t 图像:分清正逆反应,分清各因素(浓度、温度、压强、催化剂)对反应速率和平衡移动的影响。?二、平衡图像 1.出现拐点的图像:分析依据“先拐先平”。在转化率-时间图像或物质的百分含量-时间图像中,先出现拐点的曲线先达到平衡(代表温度高或压强大或使用合适的催化剂等)。
本题难度:一般
3、填空题 (1)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因?;加入石膏(CaSO4 2H2O)可以使土壤碱性降低,有关反应的化学方程式为?。
2H2O)可以使土壤碱性降低,有关反应的化学方程式为?。
(2)在一定条件下进行如下反应:aX(g)+bY(g)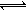 cZ(g)
cZ(g)
右图是不同温度下反应达到平衡时,反应混合物中Z的体积分数?和压强关系示意图。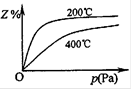
① 写出该反应的化学平衡常数表达式:K=?。随着温 度的升高,K值?(填“增大”、“减小”或“不变”)。当反应物起始浓度相同时,平衡常数K值越大,表明?(字母填序号)。
A.X的转化率越高
B.反应进行得越完全
C.达到平衡时X的浓度越大
D.化学反应速率越快
② 如右图所示,相同温度下,在甲、乙两容器中各投入1molX、2molY和适量催化剂,甲乙两容器的初始体积均为1L,甲、乙容器达到平衡所用时间:甲?乙(填“>”、“<”或“=”,下同),平衡时X和Y的转化率:甲?乙。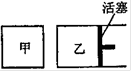
参考答案:(1)CO32-+H2O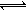 HCO3-+OH―? HCO3-+H2O
HCO3-+OH―? HCO3-+H2O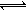 H2CO3+OH―
H2CO3+OH―
CaSO4 2H2O+Na2CO3=CaCO3↓+Na2SO4+2H2O?
2H2O+Na2CO3=CaCO3↓+Na2SO4+2H2O?
(2)① 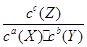 ?减少? AB
?减少? AB
② >?<
本题解析:(1)土壤呈碱性的原因是由于CO32-和HCO3的水解产生了OH―,其离子方程式为:
CO32-+H2O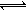 HCO3-+OH―和 HCO3-+H2O
HCO3-+OH―和 HCO3-+H2O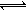 H2CO3+OH―;加入石膏(CaSO4
H2CO3+OH―;加入石膏(CaSO4 2H2O),Ca2+可以跟CO32-生成溶解度很小的CaCO3,促进上述平衡向坐移动,从而使土壤碱性降低,有关反应的化学方程式为:CaSO4
2H2O),Ca2+可以跟CO32-生成溶解度很小的CaCO3,促进上述平衡向坐移动,从而使土壤碱性降低,有关反应的化学方程式为:CaSO4 2H2O+Na2CO3=CaCO3↓+Na2SO4+2H2O ;(2)①对于aX(g)+bY(g)
2H2O+Na2CO3=CaCO3↓+Na2SO4+2H2O ;(2)①对于aX(g)+bY(g)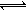 cZ(g),其化学平衡常数表达式:K=
cZ(g),其化学平衡常数表达式:K=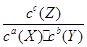 ,由图可以看出该反应是放热反应,所以温度升高,K值减少;当反应物起始浓度相同时,平衡常数K值越大,说明反应进行得越完全,同时X或者是Y的转化率越高,故选AB;②由反应混合物中Z的体积分数和压强关系示意图还可以看出,a+b>c,当甲乙两容器的初始体积均为1L时,由于甲是固定体积,乙的体积可变化,又a+b>c,所以乙的反应速率大,达到平衡的时间短,所以所用时间:甲>乙,同样又由于a+b>c,甲的转化率<乙。
,由图可以看出该反应是放热反应,所以温度升高,K值减少;当反应物起始浓度相同时,平衡常数K值越大,说明反应进行得越完全,同时X或者是Y的转化率越高,故选AB;②由反应混合物中Z的体积分数和压强关系示意图还可以看出,a+b>c,当甲乙两容器的初始体积均为1L时,由于甲是固定体积,乙的体积可变化,又a+b>c,所以乙的反应速率大,达到平衡的时间短,所以所用时间:甲>乙,同样又由于a+b>c,甲的转化率<乙。
点评::该题考查化学平衡的移动,是高考的考查重点,该题的信息量较大,但是难度不大。
本题难度:困难
4、选择题 有A、B两个起始容积相等的恒温密闭容器,A保持恒压,B保持恒容.起始时向A、B中均通入2molSO2和1molO2后,在一定条件下反应达到平衡.则下列说法中不正确的是
A.达到平衡时,SO2的转化率:A<B
B.起始时的反应速率:A=B,反应完成时的平均速率:A<B
C.达到平衡后再充入等量氦气,A、B中平衡均不发生移动
D.若再向A中充入2molSO3,平衡时SO2的质量分数不变
参考答案:BCD
本题解析:2SO2+O2 2SO3属于正反应气体系数减小的可逆反应,反应进行时气体的总物质的量减小,A容器恒压,容器内气体的压强不变,而B容器恒容,容器内气体的压强减小,故A相对于B来说,相当于加压
2SO3属于正反应气体系数减小的可逆反应,反应进行时气体的总物质的量减小,A容器恒压,容器内气体的压强不变,而B容器恒容,容器内气体的压强减小,故A相对于B来说,相当于加压
A:加压,平衡正向移动,SO2的转化率增大,故A>B,不正确
B:起始时两容器反应状态完全相同,反应速率相等,反应完成时,A容器内压强大,反应速率快,即A>B,不正确
C:达到平衡后再充入等量氦气,A容器相当于减压,平衡左移,而B容器内各物质的浓度不变,正逆反应速率仍旧相等,平衡不移动,不正确
D:在恒压情况下,若再向A中充入2molSO3,与原平衡等效,平衡时SO2的质量分数不变,正确
故答案为BCD
本题难度:一般
5、选择题 对于3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
A.K=
B.K=
C.K=
D.K=
参考答案:D
本题解析:略
本题难度:简单