时间:2019-06-28 21:35:14
1、选择题 向盛有乙醇的烧杯中投入一小块金属钠,可以观察到的现象是( )
A.钠块沉在乙醇液面下面
B.钠块熔成小球
C.钠块在乙醇液面上游动
D.钠块表面有气泡生成
参考答案:AD
本题解析:
本题难度:简单
2、填空题 (8分)0.2mol有机物与0.5molO2恰好完全燃烧后的产物为CO2和H2O(g)。产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过碱石灰剩余气体被完全吸收,碱石灰质量增加17.6g。
(1)燃烧后产物的物质的量分别为CO2________mol、H2O(g)__________mol。
(2)推断该有机物的分子式为_____________。
(3)若0.2mol该有机物恰好与9.2g金属钠完全反应,其核磁共振氢谱显示只有两种不同环境的H,试确定该有机物的结构简式为____________。
参考答案:(8分)①0.4?0.6(各2分)?②C2H6O2(2分)?③HOCH2CH2OH(2分)
本题解析:略
本题难度:简单
3、简答题 一氯甲烷的某些物理数据如下表:
熔点
℃
沸点
℃
液态时
密度
g/cm3
18℃时在水中的溶解度
mL/L
乙醚、丙酮
或苯中的
溶解性
乙醇
中的
溶解性
-97.73
-24.2
0.9159
280
互溶
能溶
在实验室里可用下图装置制备一氯甲烷: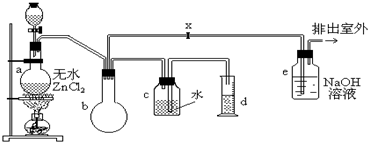
制备装置的分液漏斗中盛有甲醇,烧瓶中盛有浓盐酸.
请填写下列空白:
(1)制备一氯甲烷的化学方程式是______;该反应属于______反应.
(2)装置e中可能发生反应的化学方程式是______.
(3)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃的燃烧现象有明显区别,且生成物中有HCl).CH3Cl燃烧的化学方程式是______.
(4)装置b的作用是______.某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇和浓盐酸的量比理论计算的量多(装置的气密性没有问题),其原因是______.实验结束后,d中收集到的液体中含有______.
参考答案:(1)甲醇和氯化氢反应生成一氯甲烷和水,CH3OH+HCl→CH3Cl+H2O,甲醇中的羟基被氯原子所替代,所以属于取代反应,故答案为:CH3OH+HCl→CH3Cl+H2O;取代;
(2)一氯甲烷在氢氧化钠的水溶液中水解生成甲醇,氯化氢能与氢氧化钠发生中和反应,故答案为:CH3Cl+NaOH→CH3OH+NaCl;HCl+NaOH→NaCl+H2O;
(3)一氯甲烷与氧气反应生成二氧化碳,水和氯化氢,故答案为:2CH3Cl+3O2→2CO2+2H2O+2HCl;
(4)气体中有氯化氢,可能发生倒吸,故b为安全瓶或防止倒吸;该反应是可逆反应,不能进行到底;反应生成一氯甲烷还可能有过量的氯化氢,
故答案为:安全瓶或防止倒吸;该反应是可逆反应,不能进行到底;CH3Cl、HCl;
本题解析:
本题难度:一般
4、填空题 化学式C8H10O的化合物A具有如下性质:
①A+Na 慢慢产生气泡?②A+RCOOH
慢慢产生气泡?②A+RCOOH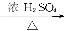 有香味的产物?③A
有香味的产物?③A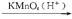 苯甲酸?④其催化脱氢产物不能发生银镜反应?⑤脱水反应的产物,经聚合反应可制得一种塑料制品(它是目前造成“白色污染”的主要污染源之一)。
苯甲酸?④其催化脱氢产物不能发生银镜反应?⑤脱水反应的产物,经聚合反应可制得一种塑料制品(它是目前造成“白色污染”的主要污染源之一)。
试回答:
(1)根据上述信息,对该化合物的结构可作出的判断是_____________;
A.苯环上直接连有羟基
B.苯环侧链末端有甲基
C.肯定有醇羟基
D.肯定是芳香烃
(2)化合物A的结构简式_____________;
(3)A和金属钠反应的化学方程式_______________________________________。
参考答案:(1)C?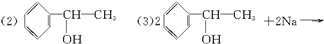
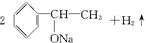
本题解析:据①②知该物质为醇,据③可知该醇分子内有一个苯环,据④知该醇分子苯环上只有一个支链,且支链上羟基不连在末端碳原子上,依据化学式为C8H10O可推知其结构简式为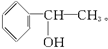
本题难度:简单
5、计算题
(1)3.40 g醇中C、H、O物质的量分别为:C___________mol、H___________mol、O___________mol;该醇中C、H、O的原子数之比为_____________。
(2)由以上比值能否确定该醇的分子式?_____________。其原因是?。
(3)如果将该多元醇的任意一个羟基换成一个卤原子,所得到的卤代物都只有一种,试写出该饱和多元醇的结构简式。_____________。
参考答案:(1)0.125? 0.300? 0.100? 5∶12∶4
(2)可以因为该醇最简式中氢原子个数已饱和,所以最简式即分子式为C5H12O4
(3)C(CH2OH)4
本题解析:醇完全燃烧,气体体积减小,此醇可构造为:(H2O)xHyCz。
(H2O)xHyCz(l)+(z+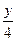 )O2(g)
)O2(g) ?zCO2(g)+(x+
?zCO2(g)+(x+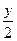 )H2O (l)
)H2O (l)
n(C)=n(CO2)=  ="0.125" mol
="0.125" mol
m(CO2)="0.125" mol×44.0 g・mol-1="5.50" g
V(C元素燃烧耗O2)=V(CO2)="2.80" L
V(H元素燃烧耗O2)="0.56" L
V总(O2)="2.80" L+0.56 L="3.36" L<5.00 L(O2过量)
m(O2)= 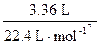 ×32.0 g・mol-1="4.80" g
×32.0 g・mol-1="4.80" g
m(醇)+m(O2)=m(CO2)+m(H2O)
m(H2O)="3.40" g+4.80 g-5.50 g="2.70" g
n(醇中H)=2n(H2O)=2×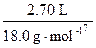 ="0.300" mol
="0.300" mol
n(醇中O)=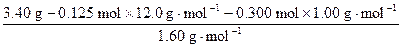 ="0.100" mol
="0.100" mol
该醇中C、H、O原子个数比为:N(C)∶N(H)∶N(O)="0.125" mol∶0.300 mol∶0.100 mol =5∶12∶4
(2)该醇最简式为C5H12O4。式中H原子已饱和,所以它本身就是醇分子式。
(3)由题意C5H12O4为四元醇,且羟基所处的位置是等同的,符合要求的只有季戊四醇,即C(CH2OH)4。
本题难度:一般