时间:2019-06-28 21:25:37
1、选择题 将pH为5的硫酸溶液稀释500倍,稀释后溶液中c (SO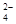 )∶c(H+)约为( )。
)∶c(H+)约为( )。
A.1∶1
B.1∶2
C.1∶10
D.10∶1
参考答案:C
本题解析:pH为5的硫酸溶液中氢离子浓度是10-5mol/L,则c (SO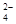 )=5×10-6mol/L,所以稀释500倍后,c (SO
)=5×10-6mol/L,所以稀释500倍后,c (SO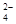 )=1×10-8mol/L。但硫酸无论怎么稀释,氢离子浓度不能小于10-7mol/L,只能是接近10-7mol/L,稀释后溶液中c (SO
)=1×10-8mol/L。但硫酸无论怎么稀释,氢离子浓度不能小于10-7mol/L,只能是接近10-7mol/L,稀释后溶液中c (SO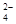 )∶c(H+)约为1∶10,答案选C。
)∶c(H+)约为1∶10,答案选C。
点评:该题是基础性试题的考查,试题灵活性强,注重考查学生的灵活应变能力和逻辑推理能力。该题的关键是明确如果酸无限稀释时,必须考虑到水的电离,然后结合提高信息灵活分析、判断即可。
本题难度:一般
2、填空题 某温度下,纯水中由H2O电离出的c(H+)=2×10-7mol·L-1,则此时H2O电离出的c(OH-)=__________mol·L-1,该温度下,浓度为0.01 mol·L-1的NaOH溶液的pH=__________。
参考答案:2×10-7? 12-lg4
本题解析:纯水中H2O电离出的c(H+)=c(OH-),所以c(OH-)=2×10-7mol·L-1,该温度下水的离子积KW=c(H+)·c(OH-)=4×10-14,浓度为0.01 mol·L-1的NaOH溶液中c(H+)=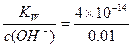 =4×10-12,pH=-lgc(H+)=12-lg4
=4×10-12,pH=-lgc(H+)=12-lg4
本题难度:简单
3、填空题 (14分)甲、乙、丙均为可溶于水的固体,可能含有的离子如下表所示:
已知:
①甲、乙的水溶液均呈碱性,丙的水溶液呈酸性;
②取一定量甲、乙、丙固体混合物,加足量水溶解,最终得到无色澄清溶液;
③向②中所得溶液逐滴加人盐酸至过量,开始无沉淀,后有沉淀生成,继续滴加沉淀消失,过程中有无色无味气体逸出;
④向丙溶液中滴加BaCl2溶液,有白色沉淀生成;
⑤将甲溶液与丙溶液混合,生成白色沉淀和无色气体。
(1) 甲、乙、丙的化学式分别为____________
(2) 250C时,PH均为12的甲溶液和乙溶液中,由水电离出来的c(OH-)之比为______。
(3) 写出⑤中发生反应的离子方程式____________
(4) 250C时,将a mol/L CH3COOH溶液与0.02 mol/L乙溶液等体积混合,所得溶液呈中性,则混合溶液中c(CH3COO-)="______" (忽略混合时溶液体积的变化)。
(5) 等物质的量浓度的乙溶液和丙溶液混合充分反应后,沉淀中的金属元素与溶液中该
元素的质量相等,则乙溶液和丙溶液的体枳比可能为______ (填选项字母)。
A.3:1
B.1:3
C.7:1
D.1:7
参考答案:(1)Na2CO3? NaOH? Al2(SO4)3?(各2分,共6分)
(2)1:10-10?(2分)?
(3)2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑(2分)
(4)0.01mol/L?(2分,不写单位扣1分)?
(5)AC (2分,每项1分,错选1个扣1分)
本题解析:丙溶液显酸性,且向丙溶液中滴加BaCl2溶液,有白色沉淀生成,所以丙中含有SO42-。将甲溶液与丙溶液混合,生成白色沉淀和无色气体,这说明二者水解相互促进,所以丙是硫酸铝。根据②③可知混合液中含有CO32-和AlO2-,因此甲是碳酸钠,乙是氢氧化钠。
(1)见答案
(2)碳酸钠水解显碱性,促进水的电离。氢氧化钠是强碱,抑制水的电离,所以水电离出来的c(OH-)之比为10-2︰10-12=1:10-10。
(3)铝离子水解显酸性,碳酸钠水显碱性,二者相互促进,方程式为2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑。
(4)溶液显中性,则根据电荷守恒可知c(CH3COO-)=c(Na+)=0.02 mol/L÷2=0.01mol/L。
(5)如果硫酸铝过量,则溶液中是铝离子,根据方程式Al3++3OH-=Al(OH)3↓可知,氢氧化钠的物质的量和硫酸铝的物质的量是3︰1。如果氢氧化钠过量,则方程式为Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O,所以氢氧化钠的物质的量和硫酸铝的物质的量是7︰1,答案选AD。
本题难度:一般
4、填空题 下列是酸溶液与碱溶液发生反应的各种关系,请用“>”“<”或“=”填空:?
(1) 取0.2 mol/LHX溶液与0.2 mol/L NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(X-)。
①混合溶液中c(HX)? c(X-);?
②混合溶液中c(HX) + c(X-)? 0.1 mol/L(忽略溶液体积变化);?
③混合溶液中由水电离出的c(OH-)? 0.1 mol/L 的HX溶液中由水电离出的c(H+)。
(2) 如果取0.2 mol/LHX溶液与0.1 mol/LNaOH溶液等体积混合,测得混合溶液的PH>7,则说明在相同浓度时HX的电离程度? NaX的水解程度。
(3) 分别取pH=2的硫酸和醋酸各50mL,加入足量的镁粉,反应开始时,反应速率前者_________后者;充分反应后,相同条件下产生氢气的体积前者_________后者。
(4) 等浓度等体积的盐酸和醋酸,分别与等浓度的NaOH溶液反应,恰好中和时,消耗NaOH的体积前者__________后者,所得溶液的pH前者________后者。
参考答案:(1) <;="?" ;> ;
(2) ?<;
(3) ?=,<;?
(4) ?=,<;(每空1分)
本题解析:略
本题难度:简单
5、选择题 已知两种弱酸HA、HB的电离平衡常数Ka(HA)>Ka(HB)。下列有关说法正确的是
A.等温浓度均为0.1 mol·L-1的HA、HB溶液中,其溶液的pH大小为:pH(HA)>pH(HB)
B.在0.1mol·L-1的NaA溶液中各离子浓度关系为:c(Na+)>c(A-)>c(OH-)>c(H+)
C.等体积pH相同的HA、HB溶液,分别加入等浓度的NaOH溶液,恰好完全反应消耗的NaOH溶液体积HA比HB多
D.等温浓度均为0.1 mol·L-1的NaA、NaB溶液中,其溶液的pH大小为:pH(NaA)>pH(NaB)
参考答案:B
本题解析:电离平衡常数越大,酸越强,相应的钠盐水解程度就小,所以AD不正确,B正确.pH相同时,HB的浓度大,则消耗的氢氧化钠多,C不正确。答案选B。
本题难度:一般