时间:2019-06-28 21:22:31
1、选择题 下列实验设计和结论相符的是?(?)
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
C.某无色溶液中加Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,则原溶液中一定有SO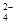
D.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
参考答案:D
本题解析:选项A:萃取必须两种溶剂互不溶解,但乙醇能溶解在水中,故错误。选项B:
加热会使氯化铁水解,得不到纯净的氯化铁溶液。选项C:若原溶液含有SO32_,加入稀盐酸
后生成硝酸具有强氧化性,能把亚硫酸根氧化成硫酸根,所以无法判断原溶液一定含有硫酸
根。
点评:本题是对化学综合实验的考查,解题过程中要求考生熟练掌握课本的相关知识,如萃
取操作、除杂操作、离子的检验等。
本题难度:简单
2、填空题 有以下实验装置可供选择: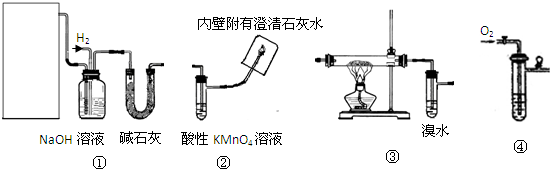
Ⅰ、实验室用甲醇催化氧化法得到甲醛,并验证甲醛的性质.请回答下列问题:
(1)应选择的装置是______(填写编号);
(2)若③硬质玻璃管中装有铜粉,请写出硬质玻璃管中发生反应的化学方程式______;______
(3)实验结束后,观察到溴水褪色.为解释这一现象,某学习小组的同学提出两种猜想:
A.发生了加成反应;
B.发生了氧化反应.为探究哪种猜想正确,学习小组的同学用pH计测溴水褪色前后溶液的pH.测得溶液的pH下降,试写出褪色的化学方程式______
Ⅱ、若选择①③②验证乙烯与氢气反应产物,请回答下列问题:
(4)写出实验室制乙烯的化学方程式______;
(5)NaOH溶液的作用是______;
(6)实验过程中,发现③中溴水褪色,试用化学方程式表示溴水褪色的原因______;
(7)出现什么现象可说明乙烯与氢气反应生成了乙烷______.
参考答案:I、(1)根据实验目的是用甲醇催化氧化法得到甲醛,并且验证甲醛性质,需要与氧气加热反应,所以选装置③④,
故答案为:③④(或④③);
(2)发生反应有甲醇催化氧化和溴水与生成的甲醛发生加成反应,反应的方程式为:CH3OH+O2催化剂
本题解析:
本题难度:一般
3、实验题 兴趣小组通过实验探究溶解铜的方法和本质。
(1)在热水浴中进行3个实验,部分实验报告如下表所示。 
①实验I、Ⅱ的目的是____________。
②实验Ⅲ中反应的本质是(用离子方程式表示)____________________。
(2)利用电化学原理实现铜溶于稀硫酸并生成氢气。
①Cu作_______极。②总反应的离子方程式是________________。
参考答案:(1)①证明Cu不与H+、NO3-单独反应;②3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(2)①阳;②Cu+2H+ Cu2++H2↑
Cu2++H2↑
本题解析:
本题难度:一般
4、实验题 “白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
方案一:取三块镀锌铁皮(A.B.C,截自同一块镀锌铁皮),将镀锌铁皮A放入烧杯中,加入40mL
6mol・L-1盐酸,反应时用玻璃棒小心翻动镀锌铁皮,待锌镀层反应完全时,立即将未反应的铁皮取出,洗涤.小心烘干.称量。将B.C重复上面的实验。
(1)锌镀层完全反应的标志是________________________________
(2)如何检验铁片已经洗净?________________________________
方案二:已知锌与强碱溶液反应的离子方程式为:Zn+2OH-+2H2O=[Zn(OH)4]2-+H2↑。某同学按下图装置设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为Scm2.质量为mg的镀锌铁皮放入
6mol・L-1 NaOH溶液中。回答下列问题: 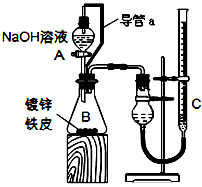
(3)装置中导管a的作用是________________________________
(4)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;②待B中不再有气体产生并恢复至室温;
③由A向B中滴加足量NaOH溶液;④上下移动C,使干燥管和C中液面相平。
上述操作的顺序是__________________(填序号)。
参考答案:(1)反应速率突然减小
(2)取最后一次洗出液,滴加AgNO3溶液,若无白色沉淀,则铁片已洗净(或用玻璃棒蘸取最后一次洗出液,滴在蓝色石蕊试纸上,若不变红色,则铁片已洗净)
(3)使分液漏斗和锥形瓶内气压相同,NaOH溶液能顺利滴下
(4)④①③②④①
本题解析:
本题难度:困难
5、填空题 (每空1分,共12分)
(1)浓硫酸与木炭粉在加热条件下的化学方程式为____________。
(2)已知酸性KMnO4溶液可以吸收SO2,试用图4-6所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号): __________→__________→__________→__________。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是________,B瓶溶液的作用是_________,C瓶溶液的作用是_________________________。
(4)装置②中所加的固体药品是_______________,可确证的产物是_______。
(5)装置③中所盛溶液是__________,可验证的产物是__________。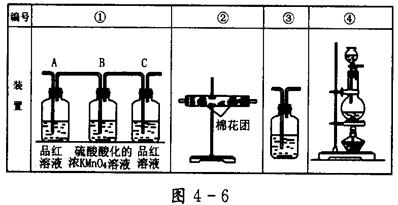
参考答案:(1)2H2SO4+C2SO2↑+ CO2↑+2H2O ?(2)④②①③?(3)检验SO2?
除去SO2?检验SO2是否除尽? (4)无水CuSO4? H2O ?(5)Ca(OH)2溶液? CO2
本题解析:(1)浓硫酸具有强氧化性,和碳的反应的方程式为2H2SO4+C2SO2↑+ CO2↑+2H2O。
(2)生成物有三种:CO2、SO2、水蒸气。由于检验CO2和SO2均需要通过溶液,所以要首先检验水蒸气,一般用无水硫酸铜来检验。检验SO2一般用品红溶液,检验CO2一般用澄清石灰水,但SO2也能是澄清石灰水变混浊,所以要在检验CO2之前先检验SO2,且在通入澄清石灰水之前还要除去SO2,吸收SO2可以用酸性高锰酸钾溶液。为了验证是否除尽,还需要再一次通过品红溶液。
本题难度:一般