时间:2019-06-28 21:00:54
1、填空题 (1)1.01×105 Pa,273℃时气态单质Xn的密度为d g/L,则X的相对原子质量为_________________。
(2)相同状况下,一定体积的X的气态氢化物HmX的质量是等体积NH3的2倍。则X的相对原子质量为_______________________________。
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为____________________。
(4)标准状况下,1体积水可以溶解700体积氨气,所得溶液的密度为0.90 g・cm-3,则所得氨水的物质的量浓度为__________________。
(5)已知98%的浓H2SO4溶液的物质的量浓度为18.4 mol/L,试判断49%的H2SO4溶液的物质的量浓度______(“大于”“小于”或“等于”)9.2 mol/L
参考答案:(1)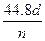 ?(2)34-m(m=1,2……)(3)
?(2)34-m(m=1,2……)(3)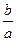 NA?(4)18.37 mol/L(5)小于
NA?(4)18.37 mol/L(5)小于
本题解析:略
本题难度:简单
2、选择题 阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是 ( )
A.常温常压下,18.0 g NH4+中所含的质子数为6.02×1024
B.250mL2mol/L的氨水中含有NH3・H2O的分子数为0.5×6.02×1023
C.1 L 1 mol/L的K2CO3溶液中离子总数大于3NA
D.1mol Cl2参加的任何反应,反应过程中转移电子数都是2NA
参考答案:C
本题解析:略
本题难度:一般
3、选择题 设NA表示阿伏加德罗常数的值,下列说法正确的是
A.5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA
B.22.4L SO2含有NA个SO2分子
C.1.6g CH4所含的电子数为NA
D.标况下,4.48L的水中含有H2O分子的数目为0.2NA
参考答案:C
本题解析:A、铁与盐酸反应后变为+2价,5.6g铁的物质的量为0.1mol,故失去0.2mol电子,A错误;B、二氧化硫气体所处的状态不明确,故无法计算二氧化硫的物质的量和分子个数,B错误;C、甲烷的物质的量n=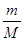 =
=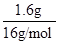 =0.1mol,而1mol甲烷含10mol电子,故0.1mol甲烷含1mol电子,C正确;D、标况下,水非气态,D错误;答案选C。
=0.1mol,而1mol甲烷含10mol电子,故0.1mol甲烷含1mol电子,C正确;D、标况下,水非气态,D错误;答案选C。
考点:考查阿伏加德罗常数。
本题难度:一般
4、选择题 有一种黄棕色气体X,其体积为20毫升,完全分解后生成10毫升的氯气和20毫升氧气(同温同压下测定),判断X为三原子分子依据的定律是(? )
①质量守恒定律?②能量守恒定律?③能量最低原理?④阿伏加德罗定律
A.①②
B.①④
C.②③
D.②④
参考答案:B
本题解析:由阿伏加德罗定律可知,在一定温度和压强下,气体的体积之比等于物质的量之比,则有:2X=Cl2+2O2,化学反应遵循质量守恒定律,则X的化学式为ClO2,为三原子分子,选A。
本题难度:一般
5、选择题 设NA代表阿伏加德罗常数的值,下列说法不正确的是(? )。
A.阿伏加德罗常数NA是0.012kg12 C中所含的原子数
B.2g氢气所含氢原子数目为NA
C.标况下,22.4L NH3所含的分子数目为NA
D.1 L 1 mo1・L-1 NaCl溶液中所含有的Na+离子数目为NA
参考答案:B
本题解析:A正确,0.012kg12 C中所含的原子数即为阿伏加德罗常数;B错,2g氢气物质的量为1mol,含氢原子数为2NA;C正确,标况下,22.4L NH3的物质的量为1mol,所含的分子数目为NA;D正确,1 L 1 mo1・L-1? NaCl溶液中NaCl的物质的量为1mol,溶液中所含有的Na+离子数目为NA;
本题难度:一般