时间:2019-06-28 20:44:49
1、选择题 标准状况下将VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρ g/mL,质量分数为w,物质浓度为c mol/L,则下列关系中不正确的是( ?)
A.ρ =" (17V+22400)" / (22.4+22.4V)
B.w =" 17c" / (1000ρ)
C.w =" 17V" / (17V+22400)
D.c =" 1000Vρ" / (17V+22400)
参考答案:A
本题解析:c=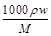 ,B正确;w=
,B正确;w=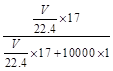 ×100%,C正确;c=
×100%,C正确;c=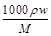 =
= 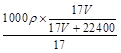 ,D正确。
,D正确。
点评:注意公式的变形和灵活运用。
本题难度:一般
2、选择题 某溶液大量含有的离子仅有: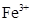 、
、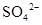 、
、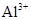 和M离子,且
和M离子,且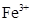 、
、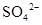 、
、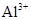 ?和M离子的物质的量之比为2:4:1:1,则M离子是( )
?和M离子的物质的量之比为2:4:1:1,则M离子是( )
A.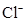
B.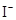
C.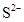
D.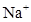
参考答案:A
本题解析:溶液为中性,阳离子所带正电荷总数与阴离子所带负电荷总数相等,设M离子的电荷为n,则:2×3―4×2+3×1+n=0,求出n=―1,因为I?能与Fe3+发生氧化还原反应,不能共存,所以只有A型Cl?符合题意。
本题难度:一般
3、填空题 在实验室配制溶液时,常涉及以下过程:①称量、量取;②过滤;③蒸发结晶、干燥;④计算;⑤溶解.
请按要求回答下列问题:
(1)甲同学用氯化钠和蒸馏水配制50 g 5%的氯化钠溶液.正确的操作顺序是:___________________.(用以上序号填空)现实验室中有10mL,50mL,100mL等不同规格的量筒,配制 上述溶液时最好选用_______mL的量筒.
(2)乙同学用10g含杂质10%的食盐(杂质不溶于水)和蒸馏水配制50g,5%的氯化钠溶液.正确的操作顺序是:____________________________.(用以上序号填空)
参考答案:(1) ④①⑤ ; 50 ; (2)⑤②③④①⑤。
本题解析:(1)甲同学用氯化钠和蒸馏水配制50 g 5%的氯化钠溶液.用固体和液体配制溶液,正确的操作顺序是计算、称量、溶解,因此代号是④①⑤;现实验室中有10mL,50mL,100mL等不同规格的量筒,配制溶液时仪器的规格越接近所配制的溶液的体积,则误差就越小,由于配制上述溶液时所需水的体积为47.5 mL,接近50mL,所以最好选用50mL的量筒;(2)食盐不纯时,会使配制的溶液小于5%.因此,先要提纯,一般步骤为:溶解、过滤、蒸发结晶.若量筒的量程过大,会造成误差:读数不准,残留在量筒内的液体较多.量程也不能小于液体体积,否则需要多次量取,同样造成误差。
考点:考查考查质量分数的溶液的配制步骤、物质的分离、提纯的操作即仪器的选择与使用的知识。
本题难度:一般
4、计算题 常温下,在27.9g水中溶解12.1 g Cu(NO3)2・3H2O,恰好达到饱和。设该溶液密度为1.20g /cm3。求:
(1)溶质的质量分数;(3分)
(2)该溶 液中NO3―的物质的量浓度;(3分)
液中NO3―的物质的量浓度;(3分)
(3)常温下,Cu(NO3)2的溶解度;(4分)
(4)将一根质量为100g的铁棒插入到该溶液中,一段时间后取出,洗净、干燥后称量,铁棒的质量变为100.2g,求此时溶液中Fe(NO3)2的物质的量浓度。(忽略溶液体积的变化)(4分)
参考答案:⑴ 23.5%(3分) ? ⑵ 3mol /L (3分)?
⑶ 30.7g (4分)? ⑷ 0.75mol/L (4分)
本题解析:略
本题难度:简单
5、选择题 实验室用NaCl固体配400 mL 1.0 mol/L NaCl溶液,下列判断不对的是(?)
A.用托盘天平称取NaCl固体23.4 g
B.应选用500 mL的容量瓶来配制此溶液
C.在转移操作中不慎将溶液洒到容量瓶外面,应该重新配置溶液
D.加蒸馏水至离刻度线1-2 cm时改用胶头滴管定容
参考答案:A
本题解析:实验室没有400ML的容量瓶,所以不能称23.4g,所以A错误。
本题难度:一般