时间:2019-06-28 20:26:16
1、填空题 25℃时,将0.01 mol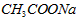 和0.002 mol
和0.002 mol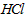 溶于水,形成1L混合溶液:
溶于水,形成1L混合溶液:
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示:
①______________________;②_______________________;③______________________。
(2)溶液中共有七种不同的粒子(指分子和离子)。在这些粒子中,浓度为0.01 mol/L的是________,浓度为0.002 mol/L的是___________;____________和____________两种粒子物质的量之和等于0.01mol。
2、填空题 工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式),操作I的名称 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是 。
③中X试剂为 。
(3)⑤的离子方程式为 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
3、填空题 (4分)0.1mol/L的HCN溶液与0.1mol/L的NaCN溶液等体积混合,混合后溶液的pH>7,说明:HCN的电离程度 CN-的水解程度;离子浓度大小顺序为 电荷守恒__________ ;物料守恒_____
4、选择题 当用标准盐酸溶液滴定待测氢氧化钠溶液时,下列操作中会使测定结果偏低的是( )
A.用酸式滴定管滴至终点时,俯视滴定管读数
B.将碱液移入锥形瓶后,加了10 ml蒸馏水再滴定
C.酸式滴定管用蒸馏水润洗后,未用标准盐酸溶液润洗
D.酸式滴定管注入酸液时,尖嘴处留有气泡,达滴定终点时气泡消失
5、选择题 下列溶液肯定显酸性的是( )
A.含H+的溶液
B.c(H+)=1×10-7mol・L-1
C.pH<7的溶液
D.c(OH-)<c(H+)的溶液