时间:2019-06-28 20:25:15
1、选择题 下列有关化学用语表示正确的是( )
A.乙炔的电子式:H:C::C:H
B.对甲基苯酚的结构简式: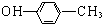
C.3,3-二甲基-1-戊烯的键线式: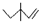
D.乙醇分子的比例模型: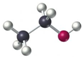
参考答案:A、乙炔分子中碳原子之间形成3对共用电子对,碳原子与氢原子之间形成1对共用电子对,电子式为 ,故A错误;
,故A错误;
B、羟基中氧原子与苯环直接相连,对甲基苯酚的结构简式为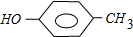 ,故B错误;
,故B错误;
C、键线式中用短线表示化学键,端点、交点是C原子,C原子、H原子不需要标出,3,3-二甲基-1-戊烯的键线式: ,故C正确;
,故C正确;
D、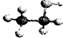 表明乙醇分子中成键情况,是乙醇的球棍模型,故D错误;
表明乙醇分子中成键情况,是乙醇的球棍模型,故D错误;
故选C.
本题解析:
本题难度:一般
2、选择题 在化合物KAl(SO4)2?12H2O中不存在的化学键是( )
A.共价键
B.非极性键
C.极性键
D.离子键
参考答案:B
本题解析:
本题难度:简单
3、选择题 下列说法正确的是( )
A.原子最外层电子数为2的元素一定处于周期表IIA族
B.主族元素X、Y能形成XY2型化合物,则X与Y?的原子序数之差可能为2或5
C.氯化氢的沸点比氟化氢的沸点高
D.同主族元素形成的氧化物的晶体类型均相同
参考答案:A.原子最外层电子数为2的元素有He、第ⅡA族元素、第ⅡB族元素等,不一定为IIA族,故A错误;
B.主族元素X、Y能形成XY2型化合物,可能有CO2、SO2、NO2、MgCl2、CaCl2等,原子序数之差可能为2、8、3或5等,故B正确;
C.氟化氢含有氢键,沸点较高,故C错误;
D.C和Si位于同一主族,但为CO2分子晶体,SiO2为原子晶体,二者晶体类型不同,故D错误.
故选B.
本题解析:
本题难度:简单
4、填空题 A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大,D、G同主族,A与B、C、D能形成电子数相同的二种常见分子,E、F的原子序数之和是D的原子序数的3倍,D、E、F的简单离子具有相同电子层结构.
(1)三种元素的名称.B______,D______,F______.
(2)A与D、A与G均可形成18e-的化合物.两种化合物在水溶液中反应的化学方程式为:______
(3)A、D、E三种元素中的两种或三种形成的物质中,含有非极性键的离子化合物的电子式为:______;只含离子键的化合物的电子式为:______.
(4)E离子的半径______(填“大于”“小于”或“等于”)?F离子的半径;E?和F元素最高价氧化物对应的水化物之间反应的离子方程式为:______.
(5)写出由上述各种元素形成的粒子中与BC-电子数相等的三种分子的化学式______、______、______.
参考答案:由短周期主族元素的原子序数依次增大,A与B、C、D能形成电子数相同的二种常见分子,由常见的10e-和18e-微粒可知,则A为氢,B为碳、C为氮、D为氧;D、G同主族,则G为硫;E、F的原子序数之和是D的原子序数的3倍,D、E、F的简单离子具有相同电子层结构,由8×32=12可知,E为钠,F为铝,
(1)B为碳,D为氧,F为铝,故答案为:碳;氧;铝;
(2)A与D、A与G均可形成18e-的化合物为H2O2、H2S,H2O2具有氧化性,H2S具有还原性,二者发生氧化还原反应为H2O2+H2S=S↓+2H2O,
故答案为:H2O2+H2S=S↓+2H2O;
(3)A、D、E三种元素中的两种或三种形成的物质有Na2O2、Na2O、NaOH等,含有非极性键的离子化合物为Na2O2,其电子式为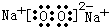
,只含离子键的化合物为Na2O,其电子式为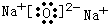
,故答案为: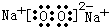
;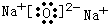
;
(4)E、F的简单离子具有相同电子层结构,原子序数大的离子半径小,则铝离子的半径小,E?和F元素最高价氧化物对应的水化物分别为NaOH、Al(OH)3,发生的离子反应为
Al(OH)3+OH-=AlO2-+2H2O,故答案为:大于;Al(OH)3+OH-=AlO2-+2H2O;
(5)BC-电子数为6+7+1=14,N2的电子数为7×2=14,CO的电子数为6+8=14,C2H2的电子数为6×2+1×2=14,故答案为:N2;CO;C2H2.
本题解析:
本题难度:一般
5、选择题 BF3与BCl3分子的空间构型均为平面正三角形,下列有关二者的比较中,正确的是
A.分子中各原子最外层都满足8电子稳定结构
B.键角均为60°,都是含有极性键的极性分子
C.BF3沸点低于BCl3沸点,因为B-F键键长短
D.BF3分子稳定性高于BCl3,因为B-F键键能高
参考答案:D
本题解析:A、分子中的B原子最外层不满足8电子稳定结构,A不正确;B、BF3与BCl3分子中B原子均不含有孤对电子,所以都是平面三角形结构,键角均为60°,都是含有极性键的非极性分子,B不正确;C、二者形成的晶体类型都是分子晶体,BF3沸点低于BCl3沸点,是因为BF3的分子间作用力小于BCl3的分子间作用力,C不正确;D、F元素的非金属性强于氯元素的非金属性,所以B-F键键能高,因此BF3分子稳定性高于BCl3,D正确,答案选D。
本题难度:一般