时间:2019-06-28 20:11:58
1、填空题 (1)常温下pH="5" HCl溶液和pH=5的AlCl3溶液中由水电离产生的c (H+) 之比等于 。
(2)写出泡沫灭火器灭火时发生反应的离子方程式 。
(3)常温下将0.01molCH3COONa和0.02mol盐酸溶于水,配成0.5L混合溶液。溶液中共有 种微粒,各离子浓度从大到小的顺序为 。
(4)常温下,向100 mL 0.01 mol・L-1HA溶液逐滴加入0.02 mol・L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(忽略溶液混合时的体积变化)。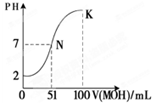
回答下列问题:
①由图中信息可知HA为_______酸(填“强”或“弱”) ② K点对应的溶液中c(M+)+c(MOH)= mol・L-1。
参考答案:(1) 10-4:1或1:104; (2)Al3++3HCO3-=Al(OH)3↓+3CO2↑
(3) 7;C(Cl-)>C(H+)>C(Na+)>C(CH3COO-)>C(OH-);(4) ①强 ②0.01
本题解析:(1)常温下pH="5" HCl的溶液,C(H+)=10-5mol/L,C(OH-)= C(H+)(水)=10-9mol/L, pH=5的AlCl3溶液C(H+)(水)=10-5mol/L 。所以二者由水电离产生的c (H+) 之比等于10-9mol/L:10-5mol/L=10-4:1=1:104. (2)泡沫灭火器灭火时发生反应的离子方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑(3)常温下将0.01molCH3COONa和0.02mol盐酸溶于水,配成0.5L混合溶液。溶液中共有H2O、CH3COOH、H+、Cl-、CH3COO-、Na+、 OH-七种微粒。HCl+CH3COONa= CH3COOH+NaCl.n(Na+)=0.01mol,n(Cl-)=0.02mol,由于CH3COOH的电离作用大于CH3COO-的水解作用,所以n(CH3COOH)>0.01mol, n(CH3COO-) < 0.01mol.n(H+)>n(OH-).各离子浓度从大到小的顺序为C(Cl-)>C(H+)> C(Na+)>C(CH3COO-)> C(OH-).(4) 100 mL 0.01 mol・L-1HA与51ml的0.02 mol・L-1MOH溶液混合溶液恰好为中性,说明HA为强酸,MOH为弱碱。K点对应的溶液中c(M+)+c(MOH)="(" 0.02 mol/L×0.1L)÷0.2L=0.01mol/L.
考点:考查酸溶液、盐溶液中水的电离、溶液中离子浓度的比较、泡沫灭火器的原理等知识。
本题难度:困难
2、选择题 现用pH=3的CH3COOH溶液和pH=11的NaOH溶液各V mL,进行中和滴定,当滴定到pH=7时,锥形瓶内溶液的体积为(滴定前后溶液未稀释、总体积不变):
A.等于2V mL
B.小于2V mL
C.大于2V mL
D.无法确定
参考答案:B
本题解析:V mLpH=3的CH3COOH溶液和pH=11的NaOH溶液V mL混合,醋酸有剩余,PH<7,所以pH=7时,消耗醋酸的体积小于V mL,故锥形瓶内溶液的体积小于2V mL,B正确。
考点:本题考查中和滴定。
本题难度:一般
3、选择题 常温下,某溶液中由水电离的c(H+)=1×10-13mol・L-1,该溶液可能是
[? ]
参考答案:A
本题解析:
本题难度:一般
4、选择题 表示下列变化的化学用语正确的是
[? ]
A.醋酸在水中电离:CH3COOH = CH3COO-+ H+
B.碳酸氢钠在水中电离:NaHCO3 = Na+ + HCO3-
C.碳酸钠在水中水解:CO32-+2H2O H2CO3 + 2OH-
H2CO3 + 2OH-
D.硫酸钡在水中电离:BaSO4 Ba2+ + SO42-
Ba2+ + SO42-
参考答案:B
本题解析:
本题难度:简单
5、选择题 常温下,对于pH = 11的NaOH溶液,下列说法错误的是
A.c(OH-) =c(Na+) + c(H+)
B.该溶液中的c(OH-) = 1.0×10-3 mol・L-1
C.与等体积pH = 3的醋酸混合后所得溶液显碱性
D.与等体积0.001 mol・L-1的氯化铵混合后所得溶液中:c(Na+)>c(NH4+)
参考答案:C
本题解析:A.根据电荷守恒可得c(OH-) =c(Na+) + c(H+),正确;B. pH = 11的NaOH溶液, c(H+)= 1.0× 10-11mol/L ,由于在室温下水的离子积是个常数,所以该溶液中的c(OH-) = 1.0×10-3 mol・L-1,正确;C.NaOH是强碱,完全电离,醋酸是弱酸,部分电离,当与等体积pH = 3的醋酸混合后由于酸过量,所以所得溶液显酸性,错误;D.与等体积0.001 mol・L-1的氯化铵混合后所得溶液爱护你以等浓度的NaCl、NH3?H2O,由于一水合氨是弱碱,部分电离,在溶液中存在电离平衡,所以c(Na+)>c(NH4+),正确。
考点:考查溶液中离子浓度大小比较、溶液酸碱性的判断的知识。
本题难度:一般