时间:2019-06-28 20:06:07
1、填空题 (12分)合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响。合成氨反应的化学方程式为:N2(g)+3H2(g)  2NH3(g) △H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。
2NH3(g) △H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。
回答下列问题:
(1)合成氨工业中原料气压缩到30~50MPa的原因是?。从平衡移动原理分析,低温有利于原料气的转化,实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,原因之二是?。
(2)500℃、50MPa时,在容积为VL的容器中加入n?mol?N2、3n?mol?H2,反应达平衡后测得平衡常数为K,此时N2的转化率为x。则K和x的关系满足K=?。
(3)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)。部
分物质的燃烧热数据如下表:
| 物?质 | 燃烧热(kJ・mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
参考答案:
(1)加压有利于平衡正向移动,提高原料气的转化率
增加反应速率,缩短达到平衡的时间?(2分)
(2)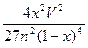 (4分)
(4分)
(3)CH4(g)+H2O(g)=CO(g)+3H2(g)?△H=+206.1 kJ・mol-1(4分)
(4)N2+6e-+8H+=2NH4+(2分)
本题解析:略
本题难度:简单
2、选择题 合成氨工业上,采用循环利用操作的主要目的是
A.加快反应速率
B.提高氨气的平衡浓度
C.降低氨气的沸点
D.提高N2和H2的利用率
参考答案:D
本题解析:略
本题难度:一般
3、填空题 海水占地球总储水量的97.2%,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。
(1)海水中存在大量的氯化钠,氯化钠中的金属元素位于元素周期表的________族。
(2)目前,国际上使用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸气,蒸气经冷却而得高纯度的淡水。由此可判断蒸馏法是________(填“物理变化”或“化学变化”)。
(3)工业上利用电解饱和食盐水可制得重要化工产品。反应式为:
NaCl+H2O NaOH+H2↑+Cl2↑(未配平),该反应中NaCl的电子式是______;利用电解所得气体制36.5%的浓盐酸1000 t,最少需消耗食盐______t。(可能用到的相对原子质量:Na:23,Cl:35.5,H:1,O:16)
NaOH+H2↑+Cl2↑(未配平),该反应中NaCl的电子式是______;利用电解所得气体制36.5%的浓盐酸1000 t,最少需消耗食盐______t。(可能用到的相对原子质量:Na:23,Cl:35.5,H:1,O:16)
(4)近年来,有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法。该方法流程如下图: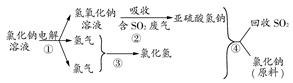
请写出②④的化学反应方程式:________、________。
参考答案:(1)ⅠA
(2)物理变化
(3) 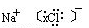 ?585
?585
(4)NaOH+SO2=NaHSO3? NaHSO3+HCl=NaCl+H2O+SO2↑
本题解析:(1)氯化钠中的金属元素为钠,它应位于元素周期表的ⅠA族。
(2)将海水蒸馏变成水蒸气属于物理变化。
(3)NaCl的电子式为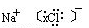 ,要制36.5%的浓盐酸1000 t所消耗的食盐应为
,要制36.5%的浓盐酸1000 t所消耗的食盐应为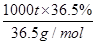 ×58.5 g/mol=585 t。
×58.5 g/mol=585 t。
(4)由图示给出的反应物和生成物不难写出②的反应方程式为NaOH+SO2=NaHSO3,④的反应方程式为NaHSO3+HCl=NaCl+H2O+SO2↑。
本题难度:一般
4、填空题 一工厂用软锰矿(含MnO2约70%及Al2O3)和闪锌矿(含ZnS约80%及FeS)共同生产MnO2和Zn(干电池原料):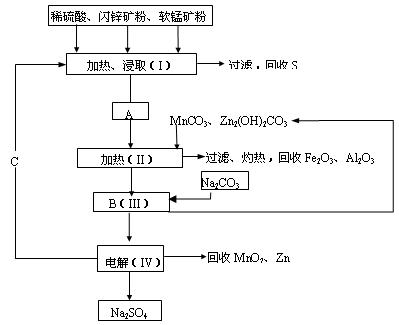
已知① A是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
② IV中的电解反应式为MnSO4+ZnSO4+2H2OMnO2+ Zn+2H2SO4。
(1)A中属于还原产物的是___________。
(2)MnCO3、Zn2(OH)2CO3的作用是_____________________________;II需要加热的原因是___________;C的化学式是____________。
(3)该生产中除得到MnO2和Zn以外,还可得到的副产品是______________。
(4)如果不考虑生产中的损耗,除矿石外,需购买的化工原料是___________。
(5)要从Na2SO4溶液中得到芒硝(Na2SO4・10H2O),需进行的操作有蒸发浓缩、________、过滤、洗涤、干燥等。
(6)从生产MnO2和Zn的角度计算,软锰矿和闪锌矿的质量比大约是__________。
参考答案:
(1)MnSO4?
(2)增大溶液的pH,使Fe3+和 Al3+生成沉淀;
使形成胶体的氢氧化铝和氢氧化铁也生成沉淀; H2SO4
(3)Fe2O3、Al2O3、S?(4)纯碱、H2SO4?(5)降温结晶?(6)1.03(或1)
本题解析:略
本题难度:简单
5、选择题 “绿色化学”提倡,设计制备物质的方案时,要从经济、环保和技术等方面考虑,以下由铜制取硝酸铜的四种方案中,比较符合“绿色化学”概念且可行的方案是( )
A.Cu→Cu(NO3)2
B.Cu→CuO→Cu(NO3)2
C.Cu→CuCl2→Cu(NO3)2
D.Cu→CuSO4→Cu(NO3)2
参考答案:B
本题解析:
本题难度:一般