ʱ��:2019-06-25 23:27:17
1��ѡ���� ��֪������CH3COOH�ĵ���ƽ�ⳣ��ΪKa�������£���20mL 0��1 mol��L��1CH3COOH��Һ����μ���0��1 mol��L��1NaOH��Һ����pH�仯������ͼ��ʾ�������¶ȱ仯��������˵���д������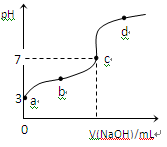
A��a���ʾ����Һ����ˮ�������H+Ũ��Ϊ1��0��10��11 mol��L��1
B��b���ʾ����Һc��CH3COO���� > c��Na����
C��c���ʾCH3COOH��NaOHǡ�÷�Ӧ��ȫ
D��b��d���ʾ����Һ��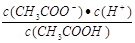 ���
���
�ο��𰸣�C
���������
��C
ǡ����ȫ��Ӧʱ������ΪCH3COONa,��ǿ�������Σ�ˮ�����Һ�ʼ��ԣ�pH>7
�����Ѷȣ�һ��
2��ѡ���� Ϊ��ʹNa2S��Һ��c(Na+)/c(S2-)�ı�ֵ��С���ɼ����������
[? ]
A����������
B������NaOH
C������KOH
D������KHS
�ο��𰸣�CD
���������
�����Ѷȣ�һ��
3��ѡ���� ��ʹ0��1mol/L��NaHCO3��Һ��c��H+����c��CO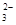 ����c��HCO3?�������٣��䷽���ǣ�?��
����c��HCO3?�������٣��䷽���ǣ�?��
A�������������ƹ���
B����ˮ
C��ͨ�������̼����
D�����뱥��ʯ��ˮ��Һ
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
4��ѡ���� ���и���Һ�У��������ʵ���Ũ�ȹ�ϵ��ȷ����
A��pH=5��NaHSO3��Һ�У�c(HSO3��)��c(H2SO3)��c(SO32��)
B��ʹ��̪�ʺ�ɫ�ı����뱽���ƻ����Һ�У�c(Na��)��c(C6H5O��)��c(OH�D)��c(H��)
C����0.1 mol��L��1 Na2CO3��Һ�У�c(HCO3��)��c(H2CO3)��c(H��)��c(OH��)
D�������ʵ���Ũ�ȡ��������NaOH��Һ��CH3COOH��Һ���������Һ�У�
c(Na��)��c(CH3COO��)��c(CH3COOH)
�ο��𰸣�BD
���������NaHSO3��Һ�����ԣ�˵������̶ȴ���ˮ��̶ȣ�����A����ȷ��ʹ��̪�ʺ�ɫ��˵����Һ�Լ��ԣ���˱����Ƶ�ˮ��̶ȴ��ڱ��ӵĵ���̶ȣ�B��ȷ��C����ȷ�������������غ㡣D��ȷ�����������غ㣬��ѡBD��
�����Ѷȣ�һ��
5��ѡ���� ����Ũ�Ⱦ�Ϊ0.1mol/L��MgCl2��Һ����ˮ��Һ���������1:2��ϡ���֪Mg(OH)2��Ksp=4.0��10��12������˵����ȷ����
A�����ǰ����ˮ��Һ��c(NH4+)��c(OH��)=1��1
B����Ϻ�c(NH4+)��c(Cl��)=1��1
C����Ϻ�c(Mg2+)��c(OH��)= 4.0��10��12
D�����Ϻ�ķ�ɢϵ�м���FeCl3��Һ����ɫ��������ɫ
�ο��𰸣�D
���������A����ˮ�д�����������ƽ�⣺NH3?H2O  NH4++OH?��H2O
NH4++OH?��H2O  H++OH?������OH?��Ũ�ȴ���NH4+��Ũ�ȣ�����B����Ϊ0.1mol/L��MgCl2��Һ����ˮ��Һ���������1:2��ϣ�����Mg(OH)2��NH4Cl����ΪNH4+ˮ�⣬����c(NH4+) < c(Cl��)������C������Ksp�ĺ��壬Ksp= c(Mg2+)��c(OH��)2= 4.0��10��12������D�����Ϻ�ķ�ɢϵ�м���FeCl3��Һ��Mg(OH)2ת��Ϊ�����ܵ�Fe(OH)3����������ɫ��������ɫ����ȷ��sp�ĺ�����Ӧ�á�����ƽ�⡢�����ˮ�⡣
H++OH?������OH?��Ũ�ȴ���NH4+��Ũ�ȣ�����B����Ϊ0.1mol/L��MgCl2��Һ����ˮ��Һ���������1:2��ϣ�����Mg(OH)2��NH4Cl����ΪNH4+ˮ�⣬����c(NH4+) < c(Cl��)������C������Ksp�ĺ��壬Ksp= c(Mg2+)��c(OH��)2= 4.0��10��12������D�����Ϻ�ķ�ɢϵ�м���FeCl3��Һ��Mg(OH)2ת��Ϊ�����ܵ�Fe(OH)3����������ɫ��������ɫ����ȷ��sp�ĺ�����Ӧ�á�����ƽ�⡢�����ˮ�⡣
�����Ѷȣ�һ��