ʱ��:2019-06-25 23:18:54
1��ѡ���� �۲����м���װ��ʾ��ͼ���й�������ȷ���ǣ�������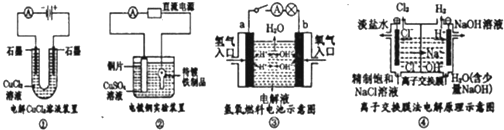
A��װ�â���������������ɫ����
B��װ�â���ͭƬӦ���Դ��������
C��װ�â������·��������b����a��
D��װ�â���������Ӧ��2?Cl--2e-=Cl2
�ο��𰸣�A������Ȼ�ͭ��Һʱ��������ͭ���ӵõ�����������ͭ���ʣ���A����
B�����ʱ���Ʋ�Ӧ���Դ�����������Ƽ����Դ��������������ͭ����������������ƷӦ���Դ������������B����
C������ȼ�ϵ���У�����������ʧ���ӣ������������õ��ӣ�����װ�â��бպϵ�������·������a������b������·��������b����a������C��ȷ��
D������װ�â��ǵ��أ������������ӵõ�����������������D����
��ѡC��
���������
�����Ѷȣ���
2��ѡ���� ����ZnƬ��CuƬ��ϡ������ɵĵ��װ���У�����һ��ʱ�乤��������˵������ȷ����
A��пƬ��������ͭƬ�������ݲ���
B�����������Ǵ�пƬ����ͭƬ
C����Һ�е��������������ƶ������������ƶ�
D�����Һ��PHֵ����
�ο��𰸣�C
���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ��п��ͭ���ã���п�Ǹ�����ͭ����������Һ�е��������������õ����ӣ����ѡ��C��ȷ��A��B����ȷ��D����ȷ����Һ�е�pH����D����ȷ����ѡC��
�����������ǻ���������Ŀ��飬Ҳ�Ǹ߿��еij������ͺͿ��㣬����������ѧ��������������������Ĺؼ�����ȷԭ��صĹ���ԭ����Ȼ���������װ��ͼ������ü��ɡ�
�����Ѷȣ�һ��
3��ѡ���� �����ϲ������Ϊԭ��صĻ�ѧ��Ӧ�ǣ�?��
A��CH4(g)��2O2(g)��CO2(g)��2H2O(1)����H��0
B��HNO3(1)��NaOH(1)��NaNO3(1)��H2O(1)����H��0
C��2H2(g)��O2(g)��2H2O(1)����H��0
D��2FeCl3(1)��Fe(s)��3FeCl2(1)����H��0
�ο��𰸣�B
���������A��Ϊ������ԭ��Ӧ����Ӧ���ȣ�����Ƴ�ԭ��أ�B��Ϊ�кͷ�Ӧ��������Ƴ�ԭ��أ�C��Ϊ������ԭ��Ӧ����Ӧ���ȣ�����Ƴ�ԭ��أ�D��Ϊ������ԭ��Ӧ����Ӧ���ȣ�����Ƴ�ԭ��ء�
�����Ѷȣ�һ��
4��ѡ���� �����������Խ��Al��Ag2O��ؿ�����ˮ�¶�����Դ����ԭ����ͼ��ʾ������˵����ȷ����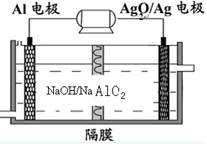
A����ظ�����Ӧʽ2Ag+2OH��-2e��=" Ag" 2O+H2O
B���ŵ�ʱ��ظ�������PH��С
C������ܷ�Ӧʽ2Al+3Ag2O+6H+ =2Al3++6Ag+3H2O
D�����Һ��Na+ͨ����Ĥ���������ƶ�
�ο��𰸣�B
�����������װ����ԭ��أ����������������缫��ӦΪAl-3e-+4OH-�TAlO2-+2H2O��AgOΪ�����������ϵĵ缫��ӦʽΪAgO+2e-+H2O�TAg+2OH-�����ܷ�ӦΪ2Al+3AgO+2NaOH�T2NaAlO2+3Ag+H2O���ŵ�ʱ����������OH-��pH��С������������OH-����������OH-����OH-�Ӹ��������������ø�ĤӦΪ�����ӽ���Ĥ��Na+����ͨ����
�����Ѷȣ�һ��
5������� ����ˮ��أ�1991���ҹ��״���������������ˮ�����Ϊ��Դ�����ͺ�ˮ��־�ƣ��Ժ�ˮΪ����ʣ��������е�����ʹ����������������������ֻҪ�ѵƷ��뺣ˮ�������ӣ��ͻᷢ��ҫ�۵İ⣬���Դ��������Ϊ��?����������Ϊ��?������������Ӧ�ֱ�Ϊ��?��?��
�ο��𰸣���������Ϊ��Al����������Ϊ��ʯī���ܵ���Ķ��Բ��ϻ�����Ա������Ľ������ϡ�
����������Ӧ��3Al��12e����3Al3��
����������Ӧ��3O2��6H2O��12e����12OH��
�������������ԭ��ع��ɵ����������ý�����������ʧȥ���ӣ�������������Ӧ�����Բ������������õ����ӣ���������ԭ��Ӧ��
�����Ѷȣ�һ��