时间:2019-06-25 23:04:48
1、选择题 下列有关元素周期表(律)说法正确的是
A.最外层有两个电子的原子一定在IIA 族
B.IA族均为碱金属
C.同一周期核电荷数越大原子半径越大
D.同一主族金属元素核电荷数越大元素金属性越强
参考答案:D
本题解析:A不正确,例如He的最外层电子数是2,属于0族。B不正确,氢元素位于第IA,是非金属。同周期自左向右原子半径逐渐减小,C不正确。同主族自上而下金属性逐渐增强,D正确,所以正确的答案是D。
本题难度:困难
2、推断题 A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B元素原子L层上的电子数为K层电子数的2倍;元素D的2价阴离子的核外电子排布与氖原子相同;E与A同主族;A和E?这两种元素与D都能形成X2Y、X2Y2型化合物。
(1)写出元素的符号:A________;B______;C________;E________。
(2)画出D的离子结构示意图____________________________。
(3)A的X2Y型化合物的电子式是_________________________。
参考答案:(1)H;C;N;Na?(2)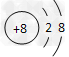
(3)
本题解析:
本题难度:一般
3、选择题 下列叙述错误的是
[? ]
A.13C和14C属于同一种元素,它们互为同位素
B.1H和2H是不同的核素,它们的质子数相等
C.14C和14N的质量数相等,它们的中子数不等
D.6Li和7Li的电子数相等,中子数也相等
参考答案:D
本题解析:
本题难度:简单
4、选择题 已知X、M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是
(甲)XO3n-+Xn-+H+→X单质+H2O(未配平);(乙)Mm++mOH-=M(OH)m↓
①若n=1,则XO3n-中X元素为+5价,X位于周期表第ⅤA族
②若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
③若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
④若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
⑤若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m
A.④⑤
B.①③
C.②③
D.①②
参考答案:C
本题解析:① +5价并不一定是该元素的最高价,所以X不一定是第ⅤA族;②若n=2,则X可能为SO32-,亚硫酸能与硫化氢发生归中反应;③若m=1,则M(NO3)m可能为硝酸银,和氨水互滴时的现象不同;④若m=2,MSO4溶液可能为FeSO4,灼烧时会被氧化成三价铁;⑤若m=3,MCl3可能为AlCl3,与足量氢氧化钠生成偏铝酸钠。
本题难度:一般
5、选择题 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间的转化关系如下图所示。下列有关物质的推断正确的是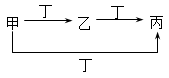
| ? | 甲 | 乙 | 丙 | 丁 |
| A | S | SO2 | SO3 | O2 |
| B | CO32― | HCO3― | CO2 | H+ |
| C | Cl2 | FeCl3 | FeCl2 | Fe |
| D | Al3+ | Al(OH)3 | AlO2― | NH3・H2O |
参考答案:B
本题解析:A、硫不能直接生成三氧化硫,错误;B、正确;C、氯气与铁反应只能生成FeCl3,错误;D、Al3+与NH3・H2O反应只能生成氢氧化铝,不能生成AlO2―,错误。
本题难度:一般