时间:2019-06-25 23:04:48
1、选择题 以下对元素非金属性的比较正确的是
[? ]
参考答案:C
本题解析:
本题难度:一般
2、推断题 已知四种元素A、B、C、D 为1~20号元素,且原子序数依次增大,A的核外电子数与其电子层数相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
请回答下列问题:?
(1) C在周期表中的位置第 ______周期,第________族;
(2)写出铜与稀HBO3溶液反应的离子反应方程式__________________;
(3)A、B形成的化合物的结构式____ ;其中含有的化学键类型为________,用电子式表示该化合物形成过程 ___________;
(4)写出D与C形成化合物的电子式____________________。
参考答案:(1)3;ⅥA
(2)“略”
(3)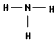 ;极性键;
;极性键;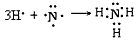
(4)“略”
本题解析:
本题难度:一般
3、选择题 元素性质随原子序数递增呈周期性变化的本质原因
A.元素的相对原子质量增大,量变引起质变
B.原子的核外电子数逐渐增加
C.原子的半径呈周期性变化
D.原子核外电子排布呈周期性变化
参考答案:D
本题解析:
本题难度:一般
4、选择题 “封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是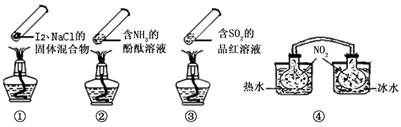
A.加热时,①上部汇聚了固体碘,说明碘的热稳定性较差
B.加热时,②、③中的溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅(已知:2NO2(g)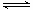 N2O4(g)△H<0)
N2O4(g)△H<0)
D.四个“封管实验”中都有可逆反应发生
参考答案:C
本题解析:A、上部聚集碘是因为碘易升华,物理性质,不是热稳定性,故A错误;B、②中为红色溶液,加热氨气逸出,溶液变无色,③中二氧化硫使品红溶液褪色,溶液为无色,加热,无色化合物分解,二氧化硫逸出,溶液变红色,故B错误;C、热水中温度升高,平衡向左移动,二氧化氮的浓度增大,颜色加深,浸泡在冷水中,温度降低,平衡向右移动,二氧化氮的浓度减小,颜色变浅,故C正确;D、①中发生的是物理变化,故没有可逆反应发生,D错误。故选C。
本题难度:一般
5、选择题 X、Y、Z是三种同周期的主族元素,它们的最高价氧化物对应水化物的酸性X>Z>Y,对下列判断不正确的是( )
A.原子半径的大小:X>Z>Y
B.气态氢化物的稳定性:X>Z>Y
C.原子序数的大小:X>Z>Y
D.元素的非金属性:X>Z>Y
参考答案:同主族元素从上到下元素的非金属性逐渐减弱,对应的最高价氧化物的水合物的酸性也逐渐减弱,X、Y、Z是三种同周期的主族元素,它们的最高价氧化物对应水化物的酸性X>Z>Y,则说明的原子序数大小关系为X<Z<Y,
A、由以上分析可知,原子序数大小关系为X<Z<Y,同主族元素从上到下,原子半径逐渐增大,故原子半径的大小为X<Z<Y,故A错误;
B、元素的非金属性越强,对应的气态氢化物的稳定性越强,已知非金属性X>Z>Y,则气态氢化物的稳定性:X>Z>Y,故B正确;
C、由以上分析可知,原子序数大小关系为X<Z<Y,故C正确;
D、X、Y、Z是三种同周期的主族元素,原子序数大小关系为X<Z<Y,同主族元素从上到下元素的非金属性逐渐减弱,则元素的非金属性:X>Z>Y,故D正确.
故选A.
本题解析:
本题难度:简单