时间:2019-06-25 23:00:19
1、选择题 取等物质的量的镁粉和铝粉混合,再将混合物平均分为四份,分别加入足量的下列溶液中,充分反应后放出氢气最多的是
A.3mol/L的HCl
B.4mol/L的HNO3
C.8mol/L的NaOH
D.18mol/L的H2SO4
2、选择题 如图示意铝在氧气中燃烧的实验,铝条点燃后,为维持燃烧继续,正确的操作是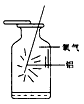
[? ]
A.铝条应始终置于集气瓶瓶口位置
B.迅速将铝条插入集气瓶接近瓶底位置
C.将铝条从瓶口位置慢慢伸向瓶底位置
D.铝条应不断上下移动
3、选择题 下列物质能与金属镁发 生反应,并产生氢气的是
生反应,并产生氢气的是
A.氯化铵溶液
B.浓硝酸
C.热的苯
D.氯化铝溶液
4、填空题 (16 分)某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验: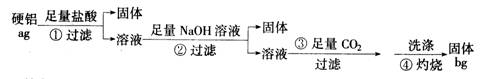
(1)补全上述①②③④各步反应的离子方程式
①?Mg+2H+===Mg2++H2↑ , ___________________________
②?_______________________, _______________________
Mg2++OH-===Mg(OH)2↓
③ ___________________________________
CO2+H20+ A102-===Al(OH)3↓+3HCO3-
④2A1(OH)3===Al203+H20
(2)该样品中铝的质量分数是(?)
(3)第②步中加入Na0H溶液不足时,会使测定结果(?)
第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果(?)
第④步对沉淀灼烧不充分时,会使测定结果(?)
A.偏高? B.偏低? C.不影响
5、填空题 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得浊液中逐渐加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。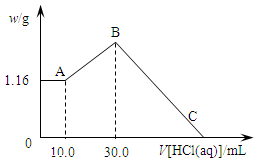
(1)A点的沉淀物的化学式为?。
(2)写出A点至B点发生反应的离子方程式:?。
(3)原混合物中NaOH的质量是?g,C点(此时沉淀恰好完全溶解)HCl溶液的体积为?mL。