时间:2019-06-25 23:00:19
1、选择题 铝、铁的混合物溶于足量的盐酸中,再加入过量的NaOH溶液,在空气中静置,当红褐色沉淀不再增加,将沉淀滤出并充分灼烧,得到的固体残留物恰好跟原混合物的质量相等,则此合金中铝的质量分数为(?)
A.22.2%
B.75.7%
C.30.0%
D.80.6%
参考答案:C
本题解析:根据题意得到的固体为Fe2O3,该物质与原混合物质量相等,所以Fe2O3中O元素的质量与混合物中Al元素的质量相等,所以合金中铝的质量分数为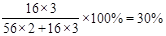 。答案选C。
。答案选C。
点评:本题主要利用质量守恒的方法进行计算,考查学生的分析能力。
本题难度:一般
2、选择题 若100 mL 0.1 mol・L-1硫酸铝溶液与氢氧化钠溶液反应,得到1.17g沉淀,则需0.5 mol・L-1NaOH溶液(?)
A.130mL
B.100mL
C.90mL
D.50mL
参考答案:AC
本题解析:
设所需NaOH溶液的体积为V。
若Al3+过量:
Al3++3OH-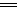 Al(OH)3↓
Al(OH)3↓
3 mol? 78 g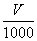 ×0.5 mol・L-1?1.17 g
×0.5 mol・L-1?1.17 g
解得V="90" mL。
若OH-过量:
Al3+ + 3OH-?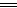 Al(OH)3↓
Al(OH)3↓
1mol ?3 mol? 78 g
0.02 mol ?0.06 mol 1.56 g
Al(OH)3+ OH-?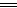
 +2H2O
+2H2O
78 g?1 mol
(1.56-1.17)g ?0.005 mol
则: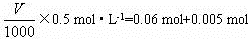
V=130mL。
本题难度:简单
3、简答题 将镁、铝的混合物0.1mol溶于100mL?2mol/L的H2S04溶液中,然后再滴加1mol/L的NaOH溶液.请回答:
(1)若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液的体积V变化如图所示.当V1=160mL时,则金属粉末中,n(Mg)=______mol,V2=______mL.
(2)若在滴加NaOH溶液的过程中,欲使Mg2+、A13+刚好沉淀完全,则滴入NaOH溶液的体积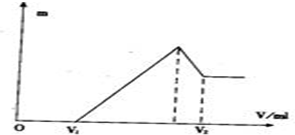
参考答案:(1)当V1=160mL时,此时,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,
由Na+离子守恒可知,n(Na2SO4)=12n(Na+)=12n(NaOH)=12×0.16L×1mol/L=0.08mol
令MgSO4为xmol,Al2(SO4)3为ymol,则:
根据Mg原子、Al原子守恒有:x+2y=0.1
根据SO42-离子守恒有:x+3y=0.2-0.08
联立方程,解得:x=0.06;y=0.02
所以金属粉末中n(Mg)=0.06mol,n(Al)=2y=2×0.02mol=0.04mol
滴加NaOH溶液到体积V2时时,溶液是Na2SO4和NaAlO2混合液,根据SO42-离子、Na+离子和Al原子守恒有:
n(NaOH)=2n(Na2SO4)+n(NaAlO2)=2n(H2SO4)+n(Al)=2×0.1L×2mol/L×+0.04mol=0.44mol,
所以,V2=0.44mol1mol/L=0.44L=440ml
故答案为:0.06mol,440?mL.
(2)当溶液中Mg2+、Al3+恰好沉淀完全时,此时,溶液是Na2SO4溶液,根据SO42-离子和Na+离子守恒有:n(Na+)=2n(Na2SO4)=2(H2SO4)=2×0.1L×2mol/L=0.4mol,所以,V(NaOH)=0.4mol1mol/L=0.4L=400ml
故答案为:400ml;
本题解析:
本题难度:一般
4、选择题 下列溶液,能用铝槽车来运送的( )
A.浓盐酸
B.浓硫酸
C.稀硫酸
D.稀硝酸
参考答案:A、铝与浓盐酸反应生成氯化铝和氢气,故不能用铝槽车来运送,故A错误;
B、铝在浓硫酸中发生钝化现象,生成一层致密的氧化物保护膜,阻止内部金属与浓硫酸继续反应,故能用铝槽车来运送,故B正确;
C、铝在稀硫酸中不能发生钝化,铝与稀硫酸反应生成硫酸铝和氢气,故不能用铝槽车来运送,故C错误;
D、铝在稀硝酸中不能发生钝化,铝与稀硝酸反应,故不能用铝槽车来运送,故D错误.
故选B.
本题解析:
本题难度:一般
5、选择题 将一定质量的Mg、Zn、Al混合物与足量稀H2SO4反应,生成H20.125mol,原混合物的质量可能是(?)
A.2g
B.4g
C.8g
D.10g
参考答案:BC
本题解析:略
本题难度:简单