时间:2019-06-25 22:41:43
1、选择题 有关理论认为N2O与CO2分子具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,下列说法合理的是
A.N2O与SiO2为等电子体、具有相似的结构(包括电子式)
B.N2O的电子式可表示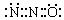
C.N2O与CO2均不含非极性键
D.N2O为三角形分子
2、选择题 下列说法中正确的是( )
A.酸性氧化物都是非金属氧化物
B.所有物质中都存在化学键
C.含有极性键的分子一定是极性分子
D.含有离子键的化合物一定是离子化合物
3、填空题 (16分)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛 应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
(1)该反应的化学方程式为?,每生成1molNF3,转移的电子数为? ?
?
生成物NF3中氮原子的杂化方式为?,NF3分子空间构型为?;
(2)N、F两种元素的氢化物稳定性比 较,NH3?HF(选填“>”或“<”);
较,NH3?HF(选填“>”或“<”);
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式??;
(4)氯化铜溶液中加入过量氨水,可以生成四氨合铜络离子,写出该反应的化学方程式?;
(5)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如左图,该离子化合物的化学式为?。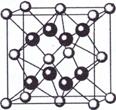
4、选择题 下列分子的结构中,原子的最外层不能都满足8电子稳定结构的是
[? ]
A.CO2
B.PCl3
C.CCl4
D.NO2
5、选择题 下列各组分子中,都属于含极性键的非极性分子的一组是( )
A.CO2、CS2
B.C2H4、CCl4
C.C60、C2H4
D.NH3、HCl