时间:2019-06-25 22:11:52
1、选择题 哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充人1mol N2和3mol H2,在一定条件下使该反应发生:N2+3H2 2NH3。下列有关说法正确的是(?)
2NH3。下列有关说法正确的是(?)
A.达到化学平衡时,正反应和逆反应的速率都为零
B.当符合:3u正(N2)=u正(H2)时,反应达到平衡状态
C.达到化学平衡时,单位时间消耗amolN2,同时生成3amolH2
D.当N2、H2、NH3的分子数比为1∶3∶2,反应达到平衡状态
2、选择题 在10 L密闭容器中,把10 mol M和10 mol N混合发生如下反应:
3M(g)+N(g) 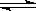 ?xP(g)+2Q(g),当反应达到平衡时,生成4 mol Q,并测得P的平衡浓度为0.4 mol・L-1,下列叙述中正确的是
?xP(g)+2Q(g),当反应达到平衡时,生成4 mol Q,并测得P的平衡浓度为0.4 mol・L-1,下列叙述中正确的是
A.M的转化率为80%
B.x的值为2
C.N的平衡浓度为0.6 mol・L-1
D.Q的体积分数为40%
3、选择题 已知某可逆反应:
mA(g) + nB(g)  pC(g)?H=" Q" kJ・mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是
pC(g)?H=" Q" kJ・mol-1,在密闭容器中进行,右图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是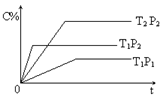
A.T1 <T2 P1>P2 m+n<P Q<0
B.T1>T2 P1<P2 m+n>P Q>0
C.T1<T2 P1<P2 m+n<P Q>0
D.T1>T2 P1<P2 m+n>P Q<0
4、填空题 (3分) 在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
5、选择题 关于下列图示的说法中正确的是 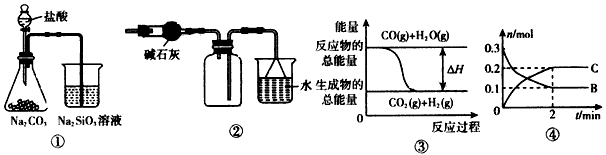
[? ]
A.由图①所示实验可得出三种元素的非金属性强弱顺序是:氯>碳>硅
B.图②可用于干燥、收集氯化氢,并吸收多余的氯化氢
C.图③表示可逆反应CO(g)+H2O(g)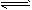 CO2(g)+H2(g)的△H>0
CO2(g)+H2(g)的△H>0
D.对反应:A(s)+2B(g)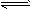 xC(g),根据图④可以求出x=2
xC(g),根据图④可以求出x=2