时间:2019-06-25 21:57:22
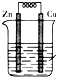
1、选择题 在图所示的原电池中,负极发生的反应是( )
A.Cu2++2e-═Cu
B.Cu-2e-═Cu2+
C.2H++2e-═H2↑
D.Zn-2e-═Zn2+
2、选择题 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是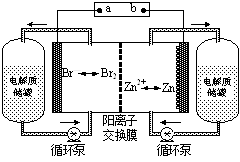
A.充电时电极a连接电源的负极
B.放电时负极的电极反应式为Zn—2e-=Zn2+
C.放电时左侧电解质储罐中的离子总浓度增大
D.阳离子交换膜可阻止Br2与Zn直接发生反应
3、选择题 某原电池的离子方程式是 Zn + Cu2+ = Zn2+ + Cu,该原电池正确的组成是
| ? | 正极 | 负极 | 电解质溶液 |
A. Cu Zn HCl B. Zn Cu CuSO4 C. Cu Zn CuSO4 D. Cu Zn ZnCl2 |
?原电池原理的应用:
1.比较不同金属的活动性强弱
根据原电池原理可知,在原电池反应过程中,一般活动性强的金属作负极,而活动性弱的金属(或能导电的非金属)作正极。
若有两种金属A和B,用导线将A和B连接后,插入到稀硫酸中,一段时间后,若观察到A极溶解,而B 极上有气体放出,说明在原电池工作过程中,A被氧化成阳离子而失去电子作负极,B作正极,则金属A的金属活动性比B强。
2.加快氧化还原反应的速率
因为形成原电池后,产生电位差,使电子的运动速率加快,从而使反应速率增大,如Zn与稀H2SO4反应制氧气时,可向溶液中滴加少量CuSO4溶液,形成Cu—Zn原电池,加快反应速率 3.用于金属的防护要保护一个铁制闸门,可用导线将其与一锌块相连,使锌作原电池的负极,铁制闸门作正极。
4.设计制作化学电源设计原电池时要紧扣构成原电池的条件。
(1)首先要将已知氧化还原反应拆分为两个半反应:
(2)然后根据原电池的电极反应特点,结合两个半反应找出正、负极材料(一般负极就是失电子的物质,正极用比负极活泼性差的金属或导电的非金属)及电解质溶液:
①电解质溶液的选择电解质溶液一般要能够与负极发生反应,或者能与电极产物发生反应。但如果两个半反应分别在两个容器中进行(中间连接盐桥),左右两个容器中的电解质溶液应选择与电极材料相同的阳离子。如在铜一锌一硫酸铜构成的原电池中,负极金属锌浸泡在含有 Zn2+“的电解质溶液中,而正极铜浸泡在含有Cu2+的溶液中.
②电极材料的选择在原电池中,选择较活泼的金属或还原性较强的物质作为负极,较不活泼的金属或能导电的非金属或氧化性较强的物质作为正极。一般,原电池的负极能够与电解质溶液反应,容易失去电子,因此负极一般是活泼的金属材料(也可以是还原性较强的非金属材料如H2、CH4等)。
(3)举例根据以下反应设计原电池:
原电池的构成条件:?
(1)活泼性不同的两个电极。
(2)电解质溶液,一般能与较活泼金属自发地进行氧化还原反应。
(3)形成闭合回路。
原电池中盐桥的作用:
盐桥中的盐溶液是电解质溶液(通常装有含琼胶的KCl饱和溶液),能使两烧杯中的溶液连成一个通路。通过盐桥中阴、阳离子的定向移动(阳离子移向正极,阴离子移向负极)维持两个半电池的电中性,以使原电池连续工作。盐桥将氧化还原反应的两个半反应隔开进行,能提高原电池的工作效率,减缓电流衰减。



原电池中的电荷流动:
在外电路(电解质溶液以外),电子(负电荷)由负极经导线(包括电流表和其他用电器)流向正极,使负极呈正电性趋势、正极呈负电性趋势。在内电路(电解质溶液中),阳离子(带正电荷)向正极移动,阴离子 (带负电荷)向负极移动。这样形成了电荷持续定向流动,电性趋向平衡的闭合电路。
| 试题ID | 试题题文 |
|---|
4、简答题 由铜片、锌片和100mL硫酸铜溶液组成的原电池工作一段时间后,铜片质量增加了12.8g,且溶液恰好变为无色.假设锌片上没有铜析出,试计算:
(1)锌片腐蚀后质量减轻了多少克?
(2)共有多少个电子流过外电路?
(3)原硫酸铜溶液的物质的量浓度是多少?
5、选择题 如图为铜锌原电池装置,下列叙述错误的是( )
A.Zn片为负极,Cu片为正极
B.Zn片上发生氧化反应
C.Cu片上发生氧化反应
D.Cu?片上有气泡产生