ʱ��:2019-06-25 21:51:30
1��ѡ���� �����£���0.1000 mol/L NaOH��Һ�ֱ�ζ�20.00 mL 0.1000 mol/L �����20.00 mL 0.1000 mol/L ������Һ���õ�2���ζ����ߣ�����ͼ��ʾ�� ����HA��ʾ�ᣬ����˵����ȷ����
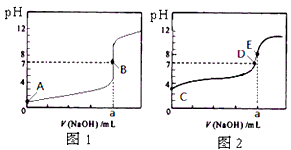
[? ]
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� �����£�����˵������ȷ����
A��������������ʵ���Ũ�ȵ�NaCl(aq) ������������NaClO(aq)����������
B��pH=3��������Һ��ˮ�ĵ���̶ȵ���pH=11�İ�ˮ��Һ��ˮ�ĵ���̶�
C��0.1 mol/L��NaHA��ҺpH��5������Һ��c(HA��)��c(H��)��c(A2��)��c(H2A)
D����NH4Cl��Һ�еμ�NaOH��Һ�����ԣ����û��Һ��c(Na��)��c(Cl��)��c(OH��)��c(H��)
�ο��𰸣�D
���������A��NaClO(aq)��NaCl(aq)�е���غ�ʽ�ֱ�Ϊc(Na��)��c(H��)=c(ClO��)��c(OH��)��c(Na��)��c(H��)=c(Cl��)��c(OH��)������NaClOˮ���Լ��ԣ������c(H��)NaClO��c(H��)NaCl������NaCl(aq)��������������NaClO(aq)������������B��������������Ũ�ȵ��ڰ�ˮ������������Ũ�ȣ����������ˮ����̶���ȣ�C��0.1?mol/L��NaHA��ҺpH=5����HA-����̶ȴ���ˮ��̶ȣ���c��A2-����c��H2A����ˮ��HA-������������ӣ���c��H+����c��A2-����HA-�ĵ����ˮ��̶ȶ���С������Һ������Ũ�ȴ�С˳����c��HA-����c��H+����c��A2-����c��H2A����D����Һ�����ԣ���c(OH��)��c(H��)�����ݵ���غ��֪c(Na��)+c(NH4+)+ c(H��)= c(Cl��) +c(OH��)������c(Cl��)�� c(Na��)���ʴ���
�����Ѷȣ�һ��
3������� ��10�֣�
�� Ũ��Ϊ0.1 mol��L��1�����ᡢ���ᡢ����������Һ���Իش�
(1)������Һ��c(H��)����Ϊa mol��L��1��b mol��L��1��c mol��L��1�����ɴ�С��˳����________��
(2)��ȫ�к�һ����NaOH��Һʱ������������������������V1L��V2L��V3L�����С��ϵΪ__________________________________��
(3)��п��Ӧ��ʼʱ�������������ʷֱ�Ϊv1��v2��v3�����ɴ�С��˳����________��
�� c(H+)��ͬ�����ᡢ���ᡢ����������Һ���Իش�
(1)������Һ����ˮϡ�������Ϊԭ����10��, c(H+)����Ϊa mol��L��1��b mol��L��1��c mol��L��1�����ɴ�С��˳����_______��
(2)������Һ�����ͬʱ,ͬʱ������ͬ��п,��������ͬ���ʵ���������������ʱ��ֱ�Ϊt1��t2��t3�����С��ϵ��___________.
�ο��𰸣����bac? ��V1=2V2=V3? ��bac ���c��a="b" ��t1=t2��t3
�����������.
��1������c(H��)=0.1mol/L������c(H��)=0.2mol/L������c(H��)��0.1mol/L����b��a��c��
��2��Ũ����ͬ�Ĵ��ᣬ���ᣬ���ᣬ���ߵ���Һ��H+Ũ�ȹ�ϵΪ���������ᣬ��Ϊ����Ϊ��Ԫ�ᣬH+Ũ��Ϊ��������H+Ũ�ȵ�2����������Ϊ���ᣬ���ֵ�������H+Ũ������С�ģ����ܵ�H+��Ũ�ȹ�ϵΪ����=������ᣬ���������Ϊǿ����ȫ���룬�����к�NaOH�������������ϵΪ����=������ᣬ��V1=2V2=V3��
��3����п��Ӧ����Ӧ��������Һ�е�H+��Ũ���йأ�H+��Ũ�ȹ�ϵΪ���������ᣬ���Գ�ʼ��Ӧ���ʹ�ϵΪ���������ᣬ��v2��v1��v3��
��.
��1��������Һ����ˮϡ�������Ϊԭ����10��, ���ᡢ������ǿ�������ȫ���룬����c(H��)����СΪԭ����1/10��������������ʣ���ˮϡ�ͻ��в����������ֵ��봦��������c(H��)�����С��ԭ����1/10����c(H��) �ɴ�С��˳����c��a=b��
��2��������Һ�����ͬʱ,ͬʱ������ͬ��п,��������ͬ���ʵ���������������ʱ���������ᡢ����c(H��)��ȡ�����t1=t2��������������ʣ�ֻ�в��������ӵ�����������ŷ�Ӧ�Ľ��У����������������ӡ����Դ���c(H��)������ᡢ����c(H��)�ʴ��ᷴӦ����ʱ����̡�t1=t2��t3��
����������ע����մ���IJ��ֵ����c(H��)��Ӱ�졣
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ���ǣ�?��
A��NaHCO3��Һ��ˮϡ�ͣ�c(Na+)/c(HCO3��)�ı�ֵ��������
B��Ũ�Ⱦ�Ϊ0.1 mol��L��1��Na2CO3��NaHCO3�����Һ��2c(Na��)��3[c(CO32��)��c(HCO3��)]
C���ڸ��������Һ�У�H+��K+��SO42���������Ƿ��ӿ��Դ�������
D����֪��Ksp(AgCl)��1.8��10��10�� Ksp(Ag2Cr2O4)��2.0��10��12����Ag2CrO4���ܽ��С��AgCl
�ο��𰸣�A
���������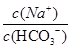 ��
��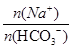 ��NaHCO3��Һ��ˮϡ��ʱ��n(Na+)���ֲ��䣬n(HCO3-)��С������c(Na+)/c(HCO3-)�ı�ֵ��������Aѡ����ȷ�����������غ㣬Ũ�Ⱦ�Ϊ0.1 mol��L��1��Na2CO3��NaHCO3�����Һ��3c(Na��)��2[c(CO32��)��c(HCO3��)]��Bѡ���������ػ����������ǣ�Cѡ�������Ag2CrO4������Һ��Ag����Ũ��Ϊx����CrO42����Ũ��Ϊ0.5x�����ܶȻ������ı���ʽ��֪Ksp��Ag2CrO4��=x2��0.5x=0.5x3=2.0��10-12��x3=4.0��10-12����x�T
��NaHCO3��Һ��ˮϡ��ʱ��n(Na+)���ֲ��䣬n(HCO3-)��С������c(Na+)/c(HCO3-)�ı�ֵ��������Aѡ����ȷ�����������غ㣬Ũ�Ⱦ�Ϊ0.1 mol��L��1��Na2CO3��NaHCO3�����Һ��3c(Na��)��2[c(CO32��)��c(HCO3��)]��Bѡ���������ػ����������ǣ�Cѡ�������Ag2CrO4������Һ��Ag����Ũ��Ϊx����CrO42����Ũ��Ϊ0.5x�����ܶȻ������ı���ʽ��֪Ksp��Ag2CrO4��=x2��0.5x=0.5x3=2.0��10-12��x3=4.0��10-12����x�T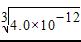 ����ΪAgCl������Һ��Ag����Ũ��Ϊ
����ΪAgCl������Һ��Ag����Ũ��Ϊ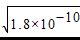 �����Ե��ܽ�ȴ���AgCl��Dѡ�����
�����Ե��ܽ�ȴ���AgCl��Dѡ�����
�����Ѷȣ�һ��
5��ѡ���� ��CH3COOH CH3COO-��H+�Ѵ�ƽ�⣬��Ҫʹ����ĵ���ƽ�������ƶ�����Һ��pHֵ����С��Ӧ������Լ���
CH3COO-��H+�Ѵ�ƽ�⣬��Ҫʹ����ĵ���ƽ�������ƶ�����Һ��pHֵ����С��Ӧ������Լ���
A��CH3COONa
B��NH3��H2O
C��HCl
D��H2O
�ο��𰸣�C
�����������CH3COONaƽ�����ƣ�PH���NH3��H2O ƽ�����ƣ�PH���HCl ƽ�����ƣ�PH��С���� H2O ���ƶ�PH���C��ȷ��
�����Ѷȣ�һ��