时间:2019-06-25 21:50:28
1、填空题 (8分)某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析: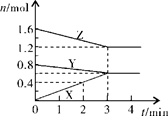
(1)该反应的化学方程式:?;
(2)反应开始至2min末,X的反应速率为??;
(3)平衡时Z的转化率为?。
(4)3min后图中曲线所表示的含义是?。
2、选择题 反应mA(g)+nB(g)?pC(g)+qD(g),经5min后达到平衡,测得此时A的浓度减少了a?mol/L,同时C的浓度增加了2a/3mol/L,又测得平均反应速率v(C)=2v(B).达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为
( )
A.2A(g)+6B(g)?3C(g)+5D(g)
B.3A(g)+B(g)?2C(g)+2D(g)
C.3A(g)+B(g)?2C(g)+D(g)
D.A(g)+3B(g)?2C(g)+2D(g)
3、填空题 在25℃时,2L的密闭容器中A、B、C三种气体的初始浓度和平衡浓度如下表:
| 物?质 | A | B | C |
| 初始浓度/mol·L-1 | 1.0 | 2.0 | 0 |
| 2min时,平衡浓度/mol·L-1 | 0.4 | 0.2 | 1.2 |

4、填空题 (9分) 在一定体积的密闭容器中,进行如下可逆化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
 ? CO2(g)+H2(g)的平衡常数K=?。
? CO2(g)+H2(g)的平衡常数K=?。 5、填空题 (5分)在密闭容器中,当合成氨的反应N2+3H2===2NH3(正反应是放热反应)达到平衡时,改变如下的一些条件:
A.升温,
B.加压,
C.减压,
D.增大c(H2),(E)减小c(NH3),(F)增大c(NH3),若平衡向右移动用“ →”,若平衡向左移动用“←”表示;若值增加用“↑”表示,若值减小用“↓”表示,请根据下表中各项的变化情况,在改变条件栏目中填上相应的编号(每项只改变一个条件)。
| 编号 | 改变条件 | 平衡移动方向 | N2的转化率 | C(NH3) | C(N2) | C(H2) |
| ① | ? | → | ↑ | ↓ | ↓ | ↓ |
| ② | ? | ← | ↓ | ↓ | ↑ | ↑ |
| ③ | ? | → | ↑ | ↑ | ↓ | ↑ |
| ④ | ? | ← | ↓ | ↓ | ↓ | ↓ |
| ⑤ | ? | → | ↑ | ↑ | ↑ | ↑ |