ʱ��:2019-06-25 21:02:45
1��ѡ���� ��ͥ���������õ��������������������������������
A.��ˮϴ�Ӻ���
B.��ˮϴ�Ӻ�δ����
C.������δϴ��
D.����ˮ��
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� ﮿��������һ�����͵Ķ��ε�أ���ŵ�ʱ�Ĺ���ԭ����ͼ��ʾ������˵����ȷ����
A���õ�طŵ�ʱ�������ķ�ӦʽΪO2��4e����4H��===2H2O
B���õ�س��ʱ������������������Ӧ��Li����e��===Li
C������е��л����Һ������ϡ�������
D��������������LiOH�ɻ�������
�ο��𰸣�D
������������⿼���˵绯ѧ֪ʶ�����ڿ��鿼���Ե绯ѧ֪ʶ�����������������������ķ�ӦʽΪO2��4e����2H2O===4OH����A�����س��ʱ������������ԭ��Ӧ��B������л����Һ������ϡ������棬��Ϊ�������ϡ�����ܷ�����Ӧ��C�����
�����Ѷȣ�һ��
3��ѡ���� ��ͼ��ʾ��a��b������ʯī����������������ȷ���� 
[? ]
A������ֽ�ϵμӷ�̪��Һ��b��������ɫ���
B��a��������������ԭ��Ӧ��b�Ǹ���������������Ӧ
C��ϡ��������������ӵ����ʵ�������
D��װ�ù���ʱ��ϡ������Һ��C(H+)��С��C(Zn2+)���
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� ����ͼ��ʾ,����������ȷ����(����)��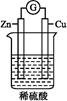
A��ͭ�Ǹ���,ͭƬ�������ݲ���
B��ͭƬ��������
C��������пƬ����������ͭƬ
D����������ͭƬ���汻��ԭ
�ο��𰸣�D
���������������Ҫ����ԭ���֪ʶ����ͼ��֪,ZnΪԭ��ظ���,ʧȥ���ӱ�����,���Ӿ�������������ͭ�缫����Һ�е��������������õ����Ӷ�����ԭΪH2��������������������෴��
�����Ѷȣ�һ��
5������� ij����ѧ��ѧ��ȤС��������ͼ��ʾԭ���װ�ý���ʵ�飬��ش��������⣺ 
��1��ʵ���У�ͬѧ�Ƿ�����װ�õ����Ƶ�ָ��ƫת����ͬ���������������¹۵㣬������ȷ����____________����˫ѡ�⣬©ѡ��2�֣���ѡ��ѡ��0�֣�
A�������������þǿ
B���������þ����ǿ����װ����þ��Ϊ����
C�������ݽ������˳����ȷ�ж�ԭ��ص�������
D��ԭ����е��������ܵ������Һ������ԡ�ǿ�����Ե����ص�Ӱ��
��2��Ҫȷ�ж�ԭ��ص����������˿��õ����Ƶ��DZ������⣬������ͨ���۲��������жϣ���д����ͼ�еĵ缫���ϼ���Ӧ������þ����Ϊ����������
������?������?��
��3��д����ͼ�еĵ缫��Ӧʽ��
�ٸ�����?_________________________��
�������� ?_________?__________?��
��4����ͼ����Ƭ��NaOH��Һ��Ӧ�����ӷ���ʽΪ___________________________________��ijͬѧ�����ͼ��ʵ��ǰ��Ƭ��������5g��ʵ����������2.3g������ʵ������в������������Ϊ_______���������ת�Ƶ��ӵ����ʵ���Ϊ________��
�ο��𰸣���17�֣���1��С��3�֣�����ÿ��2�֣�
��1��C��D(ȫ�Ե�3�֣�©ѡ��2�֣���ѡ��ѡ��0��)
��2��þƬ�������ݲ�������Ƭ�����ܽ�
��3����Mg��2e�D��Mg2��?��2H+��2e�D��H2����
(4)2Al+2OH-+2H2O��2AlO2-+3H2����3.36L��©��λ��0�֣���0.3mol��©��λ��1�֣�
�����������1����װ���У��������ϡ���ᣬ�������ǿ�Ľ����Ǹ�������װ���е����������������Һ������þ������������Һ����Ӧ������Ϊ������������þ�����������Դ�ѡCD��
��2���������Ǹ�����ʧȥ���ӣ����ܽ⡣þ����������������������ɡ�
��3����ͼ��þ�Ǹ�����������������缫��Ӧʽ�ֱ��Ǹ������ĵ缫��Ӧʽ��Mg��2e�D��Mg2�� ��������2H+��2e�D��H2����
��4����ͼ����Ƭ��NaOH��Һ��Ӧ�����ӷ���ʽΪ2Al+2OH��+2H2O��2AlO2-+3H2������ͼ��ʵ��ǰ��Ƭ��������5g��ʵ����������2.3g������������������2.7g�����ʵ�����0.1mol��ʧȥ0.3mol���ӡ�����ݵ��ӵĵ�ʧ�غ��֪�������������ʵ�����0.15mol����״���µ������0.15mol��22.4L/mol��3.36L��
�����������Ǹ߿��еij������ͺͿ��㣬�����е��Ѷ�����Ŀ��顣���������߿���������ǿ��ע�ش��������ԣ�����������ѧ������˼ά���������Ӧ������������Ĺؼ�����ȷԭ��صĹ���ԭ�����ر���ԭ��������������ж����ݣ�Ȼ��������ͷ���ʽ������ü��ɡ�
�����Ѷȣ�һ��