时间:2019-06-25 20:47:31
1、选择题 等物质的量浓度的下列溶液中,NH4+离子的浓度最大的是
A.NH4Cl
B.NH4HCO3
C.NH4HSO4
D.NH4NO3
参考答案:C
本题解析: NH4Cl、NH4NO3都是一元强酸形成的铵盐,存在NH4+的水解作用,当盐的浓度相等时,二者的水解程度相同,所以NH4+离子的浓度相同,而NH4HCO3是弱酸弱碱盐,阳离子、阴离子都发生水解反应,水解相互促进,是铵根离子水解程度比只有铵根离子的水解程度大,所以NH4+离子的浓度小于NH4Cl;NH4HSO4是二元强酸的酸式盐,电离产生的H+会抑制铵根的水解作用,使铵根离子的水解作用小于NH4Cl,所以等物质的量浓度的下列溶液中,NH4+离子的浓度最大的是NH4HSO4,选项是C。
考点:考查溶液中离子浓度的大小比较的知识。
本题难度:一般
2、选择题 下列说法错误的是
A.常温下,若醋酸钠与醋酸的混合溶液pH=7,则C(Na+)=c(CH3COO-)
B.某温度下,pH=6的NaCl溶液中离子浓度的大小关系:c(Na+)= c(Cl-)>c(H+)>c(OH-)
C.若2a mol・L-1HCN与a mol・L-1 NaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则混合溶液pH>7
D.含0.1 mol NaHCO3和0.2molNa2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO3―)+2c(CO32―)
参考答案:B
本题解析:
试题解析:溶液中一定满足c(Na+)+c(H+)=c(CH3COO-)+c(OH-),pH=7,说明溶液中氢离子与氢氧根离子浓度相等,所以c(Na+)=c(CH3COO-),故A正确;NaCl溶液 一定呈中性,c(H+)=c(OH-),故B错误;2a mol・L-1HCN与a mol・L-1 NaOH溶液等体积混合,得等浓度的HCN和NaCN溶液,若溶液中c(Na+)>c(CN-),则HCN的电离程度小于CN-的水解程度,混合溶液pH>7,故C正确;含0.1 mol NaHCO3和0.2molNa2CO3的混合液中,根据电荷守恒知:c(Na+)+c(H+)=c(OH-)+c(HCO3―)+2c(CO32―),故D正确。
考点:离子浓度的关系
本题难度:困难
3、选择题 下列说法正确的是( )
A.溶液的pH值越小,其中含有的氢离子就越多
B.物质的水溶液浓度越高,密度越大
C.单质的化学活动性越强,氧化性也越强
D.相同条件时,酸性越弱的酸,其对应的钠盐的水溶液碱性越强
参考答案:D
本题解析:
本题难度:简单
4、选择题 某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA- H++A2-。现有下列四种溶液:
H++A2-。现有下列四种溶液:
① 0.01mol?L1的H2A溶液
② 0.01mol?L1的NaHA溶液
③ 0.02mol?L1的HCl溶液与0.04mol?L1的NaHA溶液等体积混合
④ 0.02mol?L1的NaOH溶液与0.02mol?L1的NaHA溶液等体积混合
下列关于上述四种溶液的说法正确的是( )
A.溶液②中存在水解平衡:HA
参考答案:
本题解析:
本题难度:困难
5、填空题 (18分)(1)一定温度下,向1 L 0.1 mol・L-1 CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡向________(填“正”或“逆”)向移动;溶液中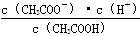 的值________(填“增大”、“减小”或“不变”)。
的值________(填“增大”、“减小”或“不变”)。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3・H2O。
已知:a.常温下,醋酸和NH3・H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3 CH3COONa+CO2↑+H2O。
CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________性,NH4HCO3溶液中物质的量浓度最大的离子是________(填化学式)。
(3)99 ℃时,Kw=1.0×10-12,该温度下测得0.1 mol・L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为_____________________________。
②该温度下,将0.01 mol・L-1 H2A溶液稀释到20倍后,溶液的pH=________。
③体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气_____。
A.盐酸多
B.H2A多
C.一样多
D.无法确定
④将0.1 mol・L-1 H2A溶液与0.2 mol・L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为_______________________________________。
参考答案:(1)逆 不变
(2)中 碱 NH4+
(3)①H2A 2H++A2-②3 ③C ④c(NH4+)>c(A2-)>c(H+)>c(OH-)
2H++A2-②3 ③C ④c(NH4+)>c(A2-)>c(H+)>c(OH-)
本题解析:(1)一定温度下,向1 L 0.1 mol・L-1 CH3COOH溶液中加入0.1 mol CH3COONa固体,因为醋酸溶液中存在CH3COOH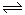 H++CH3COO-,则醋酸根离子浓度增大,平衡逆向移动;
H++CH3COO-,则醋酸根离子浓度增大,平衡逆向移动;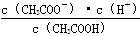 即为醋酸的电离常数,因为温度不变,所以电离常数不变;
即为醋酸的电离常数,因为温度不变,所以电离常数不变;
(2)醋酸与NH3・H2O的电离平衡常数相同,则铵根离子与醋酸根离子的水解程度相同,所以溶液呈中性;醋酸的酸性比碳酸强,所以碳酸氢根离子的水解程度大于醋酸根离子的水解程度也大于铵根离子的水解程度,碳酸氢根离子的水解使溶液呈碱性,所以碳酸氢铵溶液呈碱性;则NH4HCO3溶液中物质的量浓度最大的离子是NH4+;
(3)①99 ℃时,Kw=1.0×10-12,c(H+)=c(OH-)=10-6mol/L,因此pH=6的溶液为中性。则该温度下测得0.1 mol・L-1 Na2A溶液的pH=6,所以H2A为二元强酸,完全电离,电离方程式为H2A 2H++A2-;
2H++A2-;
②该温度下,0.01 mol・L-1 H2A溶液中氢离子的物质的量浓度是0.02mol/L,稀释到20倍后,氢离子浓度变为0.02mol/L/20=0.001mol/L,溶液的pH=-lg0.001=3;
③体积相等、pH=1的盐酸与H2A溶液中氢离子的物质的量相等,则与足量的Zn反应时产生的氢气一样多,答案选C;
④将0.1 mol・L-1 H2A溶液与0.2 mol・L-1氨水等体积混合,二者恰好完全反应生成(NH4)2A和水,铵根离子水解使溶液呈酸性,所以溶液中离子浓度的大小关系是c(NH4+)>c(A2-)>c(H+)>c(OH-)。
考点:考查电解质的电离平衡移动的判断,电离常数的判断,离子浓度的比较,电解质强弱的判断,盐的水解程度的比较,溶液酸碱性的判断
本题难度:困难