时间:2019-05-30 05:41:34
1、选择题 下列装置或操 作能达到实验目的的是
作能达到实验目的的是
A.验证反应的热效应
B.定量测定化学反应速率
C.滴定FeSO4溶液
D.构成铜锌原电池
参考答案:A
本题解析:略
本题难度:一般
2、实验题 合成氨工业对化学的国防工业具有重要意义。写出氨的两种重要用途?
?。
II. 实验室制备氨气,下列方法中适宜选用的是?。
① 固态氯化铵加热分解? ② 固体氢氧化钠中滴加浓氨水
③ 氯化铵溶液与氢氧化钠溶液共热? ④ 固态氯化铵与氢氧化钙混合加热
III. 为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(图中夹持装置均已略去)。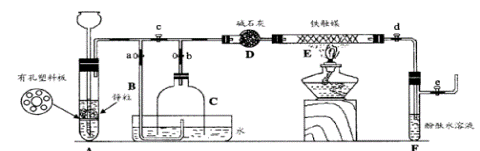
实验操作





 :
:
① 检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气发生。在F出口处收集氢气并检验其纯度。
② 关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③ 用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内水位下降到液面保持不变时打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是?。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是?,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是?,C瓶内气体的成份是?。
(3)在步骤③中,先加热铁触媒的原因是?。反应管E中发生反应的化学方程式是?。
参考答案:
I. 制化肥、制硝酸?
II. ②④
III.?(1)排除空气,保证安全
(2)锌粒与酸脱离 ; 尽量增大氢气的浓度以提高氮气的转化率; N2、H2。
(3)铁触媒在较高温度时活性增大,加快氨合成的反应速率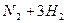

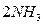
本题解析:(1)氨是一种重要的化工原料,化学工业主要来制取化肥和硝酸。
(2)氨气的实验室制法可选用固态硫酸铵获氯化铵与氢氧化钙混合加热制取,也可以采用浓氨水中加固体氢氧化钠的方法制取。但不宜采用固态氯化铵的加热分解,因为生成的氯化氢与氨气又可结合生成氯化铵。 ③不利与氨气的产生。
(3)氢气是一种易燃易爆的气体,进行加热时,要排除空气,保证氢气的纯度。问题②中C瓶内水位下降到液面保持不变时,说明A中反应停止不再产生气体,锌粒与酸分离。打开弹簧夹b,可缓冲C瓶内的压强,使氮气和氢气充分混合,增大氢气的浓度,从而提高氮气的转化率;C瓶是经氢气燃烧后,剩余气体应为氮气和氢气。问题③:铁触媒是一种催化剂,它可以加快氨合成的反应速率,它的催化性必须在较高温度下进行,所以要先加热。
本题难度:一般
3、实验题 兴趣小组的学生根据Mg与CO2反应原理推测钠也能在CO2中燃烧,为了确定其产物并进行实验论证,某同学设计了下列装置进行实验(已知PdCl2能被CO还原得到黑色的Pd)。请回答下列问题
(1)上图装置2中应盛放___________溶液(写化学式)。
(2)为了使反应随开随用,随关随停,上图方框内应选用__________装置(填上图字母代号)。
(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行1装置的操作,待装置_______(填数字编号)中出现__________现象时,再点酒精灯,这步操作的目的是____________________
(4)①若装置6中有黑色沉淀生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为______________________________。
②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为______________________________。
(5)指导老师认为,不仅要检验残留固体中是否有碳酸钠还要检验其中是否有氧化钠和碳。当确认钠充分反应后,请你设计一个简单实验,验证装置4中的残留固体中是否有Na2O和C:________________________________________________________________________________
参考答案:(1)饱和NaHCO3?
(2)C
(3)5;澄清的石灰水变浑浊;驱除系统内的空气
(4)①2Na+2CO2==Na2CO3+CO;②4Na+3CO2==2Na2CO3+C
(5)将残留固体溶于水,若有黑色不溶颗粒,则说明有碳生成;在所得水溶液中加入过量BaCl2溶液,有沉淀生成,说明有Na2CO3生成;过滤,用pH试纸检验滤液,若滤液呈碱性,则残留固体中含有Na2O
本题解析:
本题难度:困难
4、填空题 (11分)I.“阿波罗登月计划”总指挥韦伯在“阿波罗”登月成功后曾说:“阿波罗计划”中没有一项新发明的技术,都是现成的技术,关键在于综合。综合也是创新,例如可以用玻璃管制成的U形管、T形管、乳胶管、弹簧夹连接成如图所示的一种装置,在U型管中加入适量的红色溶液,即得简单U型气压计,我们可将它应用于多项实验,如:
A.证明空气中的氧气参与氧化还原反应的实验(如铁生锈);
B.溶解热效应实验(如硝酸铵溶于水);
C.装置的气密性检验实验;
D.检验某些气体性质的实验(如CO2,SO2、Cl2等与碱溶液的反应)等等。 ?
?
请从A或B中选择一项实验,画出该实验的装置图,写出实验名称。要求:①除U形气压计外,其他实验仪器或用品仅能从以下仪器中选取: 广口瓶、小试管、胶头滴管、橡皮塞、乳胶管、导管;②实验药品或试剂自定,但需在图中注明。
广口瓶、小试管、胶头滴管、橡皮塞、乳胶管、导管;②实验药品或试剂自定,但需在图中注明。
实验名称:?
Ⅱ .广口瓶简单,但它的用途真不简单!实验室用Zn粒和盐酸反应制得的H2,其中含酸雾、水汽、硫化氢及少量氧气等杂质气体,某同学仅用四只广口瓶设计了以下几种装置,按一定顺序连接,便达到了当气体通过时,每一装置除去一种气体的目的。
.广口瓶简单,但它的用途真不简单!实验室用Zn粒和盐酸反应制得的H2,其中含酸雾、水汽、硫化氢及少量氧气等杂质气体,某同学仅用四只广口瓶设计了以下几种装置,按一定顺序连接,便达到了当气体通过时,每一装置除去一种气体的目的。
(1)它们连接的顺序为________________________________;
(2)除去H2S的离子方程式为________________;
(3)除去O 2的离子方程式为________________,观察到的现象为________________。
2的离子方程式为________________,观察到的现象为________________。
参考答案:(11分)Ⅰ、(4分,画图3分,实验名称1分)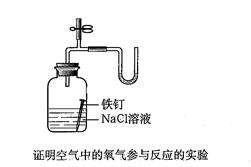
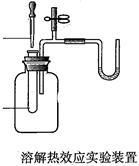
NH4NO3固体
(此装置只需画出其一即可,其他合理答案酌情给分)
Ⅱ、(最后一空1分,其余每空2分)
(1)a→b→e→f→g→h→d→c
(2) Cu2++H2S=CuS↓+2H+
Cu2++H2S=CuS↓+2H+
(3)4Fe2++O2+4H+=4Fe3++2H2O
现象:装有FeSO4和H2SO4溶液的广口瓶中溶液的颜色由浅绿色变成棕黄色
本题解析:略
本题难度:一般
5、实验题 (5分)某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出):
请回答下列问题:
(1)加热过程中,观察到A容器中出现大量白色烟雾,随着反应的进行,底部有白色沉淀生成,该沉淀物是________。
(2)对A容器中的浓H2SO4和铜片进行加热,很快发现C容器中品红溶液褪色,但始终未见D容器中澄清石灰水出现浑浊或沉淀。你的猜想是_______。设计实验验证你的猜想_____________。
参考答案:(共6分)(1)CuSO4 (1分)
(2)SO2溶解度较大,澄清石灰水中Ca(OH)2含量低,生成了Ca(HSO3)2溶液(2分。) 取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成(或者加盐酸检验SO2气体等方法)(2分。试剂或操作1分,现象描述1分)
本题解析:(1)铜和浓硫酸反应生成硫酸铜,加热的情况下,由于A容器中出现大量白色烟雾,导致溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜。
(2)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,说明产生SO2气体的速率快,但始终未见D试管中澄清石灰水出现浑浊或沉淀,这是由于SO2溶解度较大,立即生成了Ca(HSO3)2溶液的缘故。因此验证猜想的方法是取样后,向其中加入氢氧化钠溶液,观察是否有沉淀生成(或者加热、加盐酸检验SO2气体等方法)。
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。
本题难度:一般