时间:2019-05-30 05:34:36
1、选择题 将PH = 1的盐酸平均分成2份,1份加适量水,另一份加入与盐酸物质的量浓度相等的NaOH溶液后,PH均变成了2,则加入的水与NaOH溶液的体积比为
A.9
B.10
C.11
D.12
参考答案:C
本题解析:设每份盐酸的体积是V。稀释时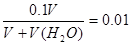 ,解得V(H2O)=9V。加氢氧化钠后,酸过量,则有
,解得V(H2O)=9V。加氢氧化钠后,酸过量,则有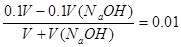 ,解得V(NaOH)=9V/11。加入的水与NaOH溶液的体积比为11︰1。答案是C。
,解得V(NaOH)=9V/11。加入的水与NaOH溶液的体积比为11︰1。答案是C。
本题难度:简单
2、选择题 下列物质的水溶液经加热浓缩,蒸干灼烧仍能得到原物质的是( )
A.FeCl3
B.Ca(HCO3)2
C.NaAlO2
D.Na2SO3
参考答案:C
本题解析:
本题难度:一般
3、选择题 有以下几种物质,①铜丝②稀H2SO4③蔗糖溶液④液态的醋酸⑤熔融的NaCl⑥氨水⑦CaCO3,其中对此分类正确的是( )
A.能导电的:①②③⑥
B.属于电解质的:②④⑤⑥
C.属于非电解质的:①③
D.属于强电解质的:⑤⑦
参考答案:A.电解质在水溶液或熔化状态下能够导电,②稀H2SO4⑥氨水分别是电解质H2SO4、一水合氨的水溶液,它们能够导电;⑤熔融NaCl中存在自由的钠离子和氯离子,能够导电;铜丝属于金属,能够导电.醋酸是电解质但是液态的醋酸不能电离出自由移动的离子不能导电,即能够导电的有②⑤⑥,故A错误;
B.电解质是指在水溶液里或熔化状态下能导电的化合物,④液态的醋酸⑤熔融的NaCl在水溶液里能导电是电解质,
⑦CaCO3是电解质,并且是强电解质.虽然它难溶于水,但溶于水的碳酸钙是完全电离的,属于电解质的:④⑤⑦,故B错误;
C.非电解质是指在水溶液里和熔化状态下都不能导电的化合物,③蔗糖溶液不导电,蔗糖溶液属于非电解质;即属于非电解质的有③,故C错误;
D.强电解质是在水溶液里完全电离的电解质,⑤NaCl水溶液里完全电离,是强电解质⑦CaCO3虽然它难溶于水,但溶于水的部分是完全电离的,属于强电解质的:⑤⑦,故D正确.
故选D.
本题解析:
本题难度:简单
4、填空题 (1)(4分)写出下列物质在水溶液中的电离方程式:
HNO3??Ba(OH)2?
NaHCO3??NaHSO4?
(2)(4分)在实验室制备氯气的过程中,多余的氯气通常是用氢氧化钠溶液进行吸收,请写出此反应的化学方程式并标出电子转移的方向和数目。?
该化学反应中,氧化剂是?,还原剂是?。
参考答案:(1)(4分)? HNO3=H++NO3–? Ba(OH)2=Ba2++2OH–
NaHCO3=Na++HCO3–? NaHSO4=Na++H++SO42–
(2)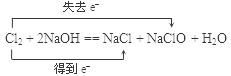 ?Cl2?Cl2
?Cl2?Cl2
本题解析:(1)酸能电离出H+和酸根离子,故HNO3电离方程式为:HNO3=H++NO3–;碱电离出金属离子和OH–,故Ba(OH)2电离方程式为:Ba(OH)2=Ba2++2OH–;弱酸的酸式盐电离时产生的是金属离子和酸式酸根离子,故NaHCO3电离方程式为:NaHCO3=Na++HCO3–;强酸的酸式盐能完全电离出H+,故NaHSO4电离方程式为:NaHSO4=Na++H++SO42–。
(2)在氯气跟氢氧化钠溶液的反应中,氯元素的化合价既降低(由0价降到–1价)又升高(由0价升到+1价),所以氯气既是氧化剂又是还原剂。
本题难度:一般
5、选择题 下列物质中属于电解质的是
A.H2
B.NH3
C.Na2SO4
D.CO2
参考答案:C
本题解析:略
本题难度:简单