时间:2019-05-30 05:32:47
1、填空题 (14分)铅蓄电池是可充电型电池,它的正负极极板是惰性材料,电池总反应式为:?
Pb+PbO2+4H++2SO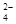
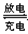 2PbSO4+2H2O
2PbSO4+2H2O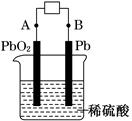
请回答下列问题(不考虑氢、氧的氧化还原):?
(1) 该蓄电池放电工作时的负极材料是?,用其电解氯化钠溶液,当阳极上收集到11.2L氯气时(标况下),理论上负极板的质量增加?g。
充电时,上图中A极应接直流电源的?(填“正极”或“负极”)。充电时A极的电极反应式是?;
(2) MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式 ? 。现以铅蓄电池为电源电解,当蓄电池中有0.4mol H+被消耗时,则电路中通过的电子的物质的量为?,MnO2的理论产量为 ? g。
参考答案:(1)铅?48,?正 ?PbSO4+2H2O-2e-= PbO2+4H++SO42-?(2)2H++2e-=H2?0.2mol? 8.7
本题解析:(1)根据电池的总反应可知,铅蓄电池放电时的负极发生氧化反应,所以负极材料为Pb,发生的电极反应为Pb-2e-+SO42-=PbSO4,因此负极增加的质量为SO42-的质量,用该电池电解氯化钠溶液时,当阳极上收集11.2L氯气时,转移1mol电子,所以负极增加48g。充电时,A极应发生氧化反应,所以与电源正极相连,电极反应为PbSO4+2H2O-2e-= PbO2+4H++SO42-。
(2)电解酸化的MnSO4溶液,阴极发生还原反应,电极反应为2H++2e-=H2。根据铅蓄电池的总反应可知,1molH2SO4参加反应转移1mol电子,所以0.4mol H+被消耗时,转移0.2mol 电子,生成MnO20.1mol,质量为8.7g。
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断。电解中最关键的是准确判断出电极上离子的放电顺序。在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,所以需要熟练记住常见离子的放电顺序。
本题难度:一般
2、选择题 我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为4Al+3O2+6H2O=4Al(OH)3。下列说法不正确的是
A.正极反应式为O2+2H2O+4e一=4OH―
B.以网状的铂为正极,可增大与氧气的接触面积
C.电池工作时,电流由铝电极沿导线流向铂电极
D.该电池通常只需更换铝板就可继续使用
参考答案:C
本题解析:A、根据电池的总反应,写出各电极的反应式:Al作负极:4Al-12e-+12OH-=4Al(OH)3,铂网作正极:3O2+6H2O+12e-=12OH-,说法正确;B、根据题目信息铂网作正极,网状的作用可增大与氧气的接触面积,说法正确;C、根据原电池的工作原理,电子从负极经导线流向正极,e-从铝经导线流向铂,而电流是从正极流向负极(铂流向的铝),说法错误;D、根据原电池的工作原理,负极不断溶解消耗,只要更换铝板就可继续使用,说法正确。
考点:考查原电池的工作原理、电极反应式的书写等相关知识。
本题难度:一般
3、选择题 在同温同压下,11。5 g气体A所占的体积和8 O2所占的体积相同,则气体A的相对分子质量为? ( )?
A.46
B.28
C.44
D.64
参考答案:A
本题解析:同温同压,相同体积的任何气体所含分子数相同,即物质的量相同;
8 O2的物质的量的为0.25mol,所以可得气体A相对分子质量为46。
本题难度:简单
4、选择题 目前人们正研究开发一种高能电池――钠硫电池,它以熔融的钠、硫为两极,以Na+导电的 陶瓷作固体电解质,反应为
陶瓷作固体电解质,反应为 ,以下说法正确的是
,以下说法正确的是
A.放电时,硫作负极,电极反应式为:  +2e-=Sx2-
+2e-=Sx2-
B.放电时,电池中消耗4.6g Na,反应中转移1.204×1023个电子
C.该反应一定是一个自发进行的吸热反应。
D.放电时,电子从钠极经外电路流向到硫极,再从硫极经内电路流向钠
参考答案:B
本题解析:A、放电时S的化合价降低,发生还原反应,作电池的正极,错误;B、放电时,电池消耗4.6gNa,物质的量是0.2mol,转移的电子数是0.2mol×6.02×1023mol-1=1.204×1023,正确;C、放电时,该反应是自发进行的放热反应,错误;D、放电时,钠作负极,S作正极,电子从钠极经外电路流向到硫极,不会从硫极经内电路流向钠,错误,答案选B。
考点:考查电化学反应原理的应用
本题难度:一般
5、填空题 (12分)(1)(6分)科学工作者为心脏病人设计的心脏起搏器使用的电池是以Pt和Zn为电极材料,依靠人体内液体中含有一定浓度的溶解氧和H+进行工作。回答下列问题:
(1)①正极材料是:?,正极反应为:?
②负极材料是:?,负极反应为:?
(2)(6分)写出下列反应的化学方程式:
①在催化剂条件下苯与液溴发生反应:
??
②乳酸(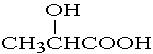 )与金属钠反应:
)与金属钠反应:
??
参考答案:(1)①? Pt (1分)? O2 + 2 H2O + 4e- ="=" 4OH-?(2分)
② Zn (1分)? 2Zn - 4e- ="=" 2 Zn2+?(2分)
(2)①?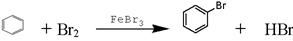 (3分)
(3分)
②? (3分)
(3分)
本题解析:略
本题难度:简单