ʱ��:2019-05-30 05:32:47
1��ѡ���� ����������ȷ����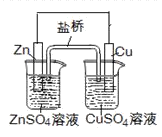
A�����ʱ��ͨ���Ѵ��ƵĽ�����Ʒ������
B����ͼZnΪ������������ԭ��Ӧ
C����ͼ������Zn�缫����Cu�缫�������е�Cl������CuSO4��Һ
D������ȼ�ϵ�أ����Ե���ʣ���O2ͨ���������缫��ӦΪ��O2+4H++4e-= 2H2O
�ο��𰸣�D
���������A�����ʱ��ͨ���Ѵ��ƵĽ�����Ʒ������������B�����ڽ������Zn>Cu,����ZnΪ����������������Ӧ������C����ͼ������Zn�缫����Cu�缫�������е�Cl����������ɽ϶��ZnSO4��Һ������D������ȼ�ϵ�أ����Ե���ʣ���O2ͨ���������缫��ӦΪ��O2+4H++4e-= 2H2O����ȷ��
���㣺����ԭ��ء����صķ�Ӧԭ����Ӧ�õ�֪ʶ��
�����Ѷȣ�һ��
2��ѡ���� ��ͼ������ȼ�ϵ�ع���ʾ��ͼ�����ڸõ�ص�˵������ȷ����
[? ]
A��a���Ǹ���
B�������ĵ缫��Ӧ�ǣ�O2+2H2O+4e-==4OH-
C��������bͨ����������a
D������ȼ�ϵ���ǻ������
�ο��𰸣�BC
���������
�����Ѷȣ�һ��
3��ѡ���� ȼ�ϵ�����������ʿɸߴ�80%�������й�ȼ�ϵ�ص�˵������?���ǣ�������
A��ȼ�ϵ�صĸ�����Ӧ�������������顢�Ҵ�������
B������ȼ�ϵ�س����ں��������������Ϊˮ��������֮��ɹ��Աʹ��
C���Ҵ�ȼ�ϵ�صĵ���ʳ���KOH��������ӦΪC2H5OH-12e-=2CO2��+3H2O
D��H2SO4������ʣ�����ȼ�ϵ�ص�������ӦΪO2+4H++4e-=2H2O
�ο��𰸣�A��ȼ�ϵ���У�ȼ����������������Ӧ����������������顢�Ҵ������ʣ���A��ȷ��
B�����������������ȼ�ϵ�صIJ�����ˮ����������֮��ɹ��Աʹ�ã���B��ȷ��
C���Ҵ�ȼ�ϵ�صĵ������KOHʱ�����ɵĶ�����̼����䷴Ӧ����̼���Σ�����������ӦC2H5OH-12e-+16OH-=2CO32-+11H2O����C����
D�������Ի����£�ȼ�ϵ����������ӦΪ��O2+4H++4e-=2H2O����D��ȷ��
��ѡC��
���������
�����Ѷȣ�һ��
4��ѡ���� ��100 mLH2SO4��CuSO4�Ļ��Һ�У���ʯī���缫���һ��ʱ�䣬�������յ�2.24L���壨��״��������ԭ���Һ�У�Cu2+�����ʵ���Ũ��Ϊ��?��?
A��1mol?L�D1? B��2mol?L�D1? C��3 mol?L�D1? D��4 mol?L�D1
�ο��𰸣�A
���������
��ȷ�𰸣�A
�ɵ����غ�ã�n(O2)��4= n(H2)��2��2n(Cu),
��0.1mol��4=0.1mol��2��2n(Cu)��
n(Cu)=0.1mol��
Cu2+�����ʵ���Ũ��Ϊ
0.1mol��0.1L?=1mol?L�D1��A��ȷ��
�����Ѷȣ���
5��ѡ���� ��ͼ��ʾ�����м׳ص��ܷ�ӦʽΪ��2CH3OH+3O2+4KOH=2K2CO3+6H2O���ڽ�ͨ��·һ��ʱ���Cu����������3.2g������˵����ȷ���ǣ�������
A���׳��ǵ���ת��Ϊ��ѧ�ܵ�װ�ã��ҳ��ǻ�ѧ��ת�����ܵ�װ��
B���׳������������ı�״���¿����������2.8?L��������O2���������20%���㣩
C����ͨ��·һ��ʱ����ҳ���CuSO4��Һ��Ũ�ȷ��������Եı仯
D���׳�ͨ��CH3OH�ĵ缫��ӦΪ��CH3OH-6e-+2H2O=CO32-+8H+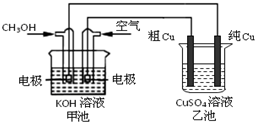
�ο��𰸣�A���׳��Ǽ״�ȼ�ϵ�أ���ԭ��صĹ���ԭ������ѧ��ת��Ϊ���ܣ��ҳ��ǵ��أ��ǵ���ת��Ϊ��ѧ�ܣ���A����
B���׳���������������Ӧ�缫��ӦΪ��O2+2H2O+4e-=4OH-���ҳ��д�ͭ�缫����ͭ�ĵ缫��Ӧ��Cu2++2e-=Cu�����ݵ���еĵ����غ㣬��Cu����������3.2g���ʵ���Ϊ0.05mol��ת�Ƶ���Ϊ0.1mol�����Լ׳���������0.025mol����״�������Ϊ0.025mol��22.4L/mol=0.56L���������Ϊ=0.56L20%=2.8L����B��ȷ��
C����ͨ��·һ��ʱ���ͭ�к�����п���Ȼ��ý���������������ʱ����ʧȥ���ӣ�ͬʱ��ͭ����������ͭ���ҳ���CuSO4��Һ��Ũ�ȷ��������Եı仯����C��ȷ��
D���׳�ͨ��CH3OH�ĵ缫��ԭ��صĸ���������������Ӧ���缫��ӦΪ��CH3OH-6e-+8OH-=CO32-+6H2O����D����
��ѡBC��
���������
�����Ѷȣ�һ��