ʱ��:2019-05-30 05:21:37
1��ѡ���� ��ʵ���ҽ��������й����ʵ��Ʊ������У���������ȷ�������Ͽ����Ҿ����Ϻ�������
[? ]
A��C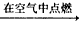 CO
CO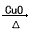 CO2
CO2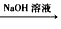 Na2CO3
Na2CO3
B��Cu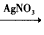 Cu(NO3)2��Һ
Cu(NO3)2��Һ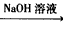 Cu(OH)2
Cu(OH)2
C��CaO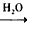 Ca(OH)2��Һ
Ca(OH)2��Һ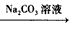 NaOH��Һ
NaOH��Һ
D��Fe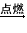 Fe2O3
Fe2O3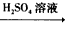 Fe2(SO4)3��Һ
Fe2(SO4)3��Һ
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� ij��ѧʵ��С������ͼ��ʾ��װ����ȡ������������������?��?��?�����Ƿ����������ʣ�����̨�����ӵ�֧������ʡ�ԣ�����֪���������ķе�Ϊ77.1�棬�Ҵ��е�Ϊ78.4�棬����ķе�Ϊ118�森�����Ҫ����գ�
��1��д��ʵ�����ñ��������ˮ�Ҵ������������Ļ�ѧ����ʽ��______��
��2��Ϊʹ��Ӧ���ַ�Ӧ�����´�ʩ����ȷ����______����д��Ӧ��ţ���
����С�����ȣ���������������״̬?���ȴ�����������״̬�����������ȱ��ַ���״̬?��ʹ��ϡ����������?������Ũ����������
��3������������ϵĵ��ܶ�һЩ���������������ռ��к�Ӱ�죬����ԭ��
��______��
��4��Aͬѧ���ռ����������������뺬��������̪��NaOH��Һ�в���ˮԡ�����ȣ�������Һ�ĺ�ɫ��dz���ɴ˵ó����������к�������Ľ��ۣ�����Ϊ��һ������ȷ��Ϊʲô��
��______��
��5��Bͬѧ���ռ����������������뱥��NaHCO3��Һ�У��۲쵽���������ݲ������ɵó��Ľ�����______���ù����з�����Ӧ�Ļ�ѧ����ʽ��______��
��6��Cͬѧ���ռ��������������������뱥��Na2CO3��Һ�У������ݲ��������ǵó������������в�������Ľ��ۣ�����������ѧ֪ʶ�����۸�ͬѧ�Ľ����Ƿ���ȷ��
�ҵ������ǣ�______��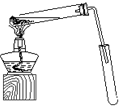
�ο��𰸣���1��������Ҵ���Ũ���������·���������Ӧ����������������ˮ����Ӧ����ʽΪCH3CH2OH+CH3COOH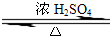
CH3COOCH2CH3+H2O��
�ʴ�Ϊ��CH3CH2OH+CH3COOH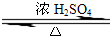
CH3COOCH2CH3+H2O��
��2��������Ҵ���Ӧ��Ũ��������������Ӧ���ӷ���Ӧ��С�����ȣ���������������״̬����ѡ���٢ܣ�
��3���ӷ�Ӧװ�ó�����Ϊ���������ܾ����������ã�������̫�̣�ʹ���������ò�����ֵ�������ʹ�ռ������٣�����Ҫ�����ȷ������õ����������
�ʴ�Ϊ��ʹ���������ò�����ֵ�������ʹ�ռ������٣�����Ҫ�����ȷ������õ����������
��4�������������ڼ��������»ᷢ��ˮ�⣬���ɵ�����Ҳ���к�NaOH�Ӷ�ʹ��̪��ɫ���ʷ�̪��ɫ���ܿ϶��Ǻ���������ɵģ�
�ʴ�Ϊ������ȷ�����������ڼ��������»ᷢ��ˮ�⣬���ɵ�����Ҳ���к�NaOH�Ӷ�ʹ��̪��ɫ���ʷ�̪��ɫ���ܿ϶��Ǻ���������ɵģ�
��5���������Ա�̼��ǿ��������̼�����Ʒ�Ӧ����Ӧ����ʽΪCH3COOH+NaHCO3=CH3COONa+CO2��+H2O��˵�����������к������ᣬ
�ʴ�Ϊ�����������к������CH3COOH+NaHCO3=CH3COONa+CO2��+H2O��
��6�������Na2CO3��Ӧ��������NaHCO3�����ų����ݣ���Na2CO3ȫ��ת��ΪNaHCO3���������NaHCO3��Ӧ����CO2���������ݣ����ԣ�û�����ݲ�����������˵�����в��������ᣮ
�ʴ�Ϊ������ȷ���������Na2CO3��Ӧ��������NaHCO3�����ų����ݣ���Na2CO3ȫ��ת��ΪNaHCO3���������NaHCO3��Ӧ����CO2���������ݣ����ԣ�û�����ݲ�����������˵�����в��������ᣮ
���������
�����Ѷȣ�һ��
3��ʵ���� ����ͼ��ʾװ�������ֲ�ͬ�����ֱ����ʵ�飬�۲�B�Թ��е����� 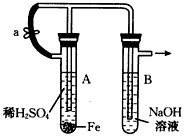
(1)����1���ȼн�ֹˮ��a����ʹA�ܿ�ʼ��Ӧ����B���й۲쵽��������________________��B�ܷ�����Ӧ�Ļ�ѧ����ʽ��_________________
(2)����2����ֹˮ��a��ʹA�ܿ�ʼ��Ӧһ��ʱ����ټн�ֹˮ��a����B���й۲쵽��������________��B���з��������ӷ���ʽ��____________________
(3)��˵���������ʵ������ͬ��ԭ��������������ͬ����С�ⲻ�ûش�________________
�ο��𰸣�(1)��ʼ������ɫ��״������Ȼ�����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��FeSO4+2NaOH=Fe(OH)3��+ Na2SO4��4Fe(OH)2+O2+2H2O=4Fe(OH)3
(2)��ֹˮ��ʱ���Թ�B�еĵ��ܿ�������ð�����н���B�в�����ɫ��״������һ��ʱ���ڳ�������ɫ��Fe2++2OH-=Fe(OH)2��
(3)����1��û���ų�B�Թ��еĿ�����������2��A�Թܲ�����H2��B�Թ��еĿ����ų�
���������
�����Ѷȣ�һ��
4��ʵ����
 ?
?�ο��𰸣���1��ȡ�������һ��ϴ����Һ������1��2��Ba(NO3)2��Һ���������ְ�ɫ���ǣ���ʾ��ϴ����ȫ��ȡ�������һ��ϴ����Һ������1��2�η�̪��Һ������Һ���Ժ�ɫ����ʾ��ϴ����ȫ�� ��2��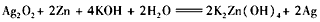
��3��91%
���������
�����Ѷȣ�һ��
5��ʵ���� ʵ���Һϳ����������IJ������£�������ƿ�ڼ����Ҵ���Ũ��������ᣬƿ����ֱ��װͨ����ȴˮ�������ܣ�ʹ��Ӧ��������������ΪҺ��������ƿ�ڣ������Ȼ���һ��ʱ�������װ�ý�����������ͼ��ʾ�����õ������Ҵ��������ˮ�����������ֲ�Ʒ����ش��������⣺
����֪���Ҵ������ᡢ���������ķе�������78.4�桢118�桢77.1�棩 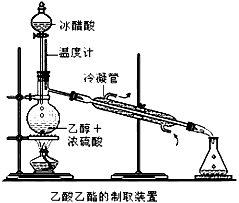
��1������ƿ�г��˼����Ҵ���Ũ����������⣬��Ӧ���뼸�����Ƭ����Ŀ����_________________________��
��2������ƿ�м���һ���������Ҵ���Ũ����Ļ��Һ�ķ����ǣ�_________________��
��3���ڸ�ʵ���У�����1mol�Ҵ���1mol ������Ũ���������¼��ȣ���ַ�Ӧ���ܷ�����1mol����������
_________________��ԭ����_________________��
��4��������뺬���ᡢ�Ҵ���ˮ�����������ֲ�Ʒ����ͼ�Ƿ��������������ͼ������ͼ��Բ�����������ʵ����Լ����ڷ������������ʵ��ķ��뷽���� 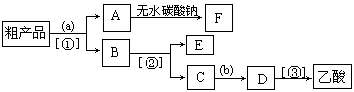
�Լ�a��__________���Լ�b��_______________�����뷽������_________________�����뷽������
__________________�����뷽������_______________��
��5���ڵõ���A�м�����ˮ̼���Ʒ�ĩ����Ŀ����_________________��
��6��д��C �� D��Ӧ�Ļ�ѧ����ʽ___________________________��
�ο��𰸣���1����ֹ��ƿ��Һ�屩��
��2��������ƿ�м���һ�������Ҵ���Ȼ��������Ũ���������ƿ���ӱ���
��3���÷�Ӧ�ǿ��淴Ӧ����Ӧ���ܽ��е���
��4������̼������Һ��Ũ�����Һ����������
��5����ȥ���������л��е�����ˮ
��6��2CH3COONa+H2SO4==Na2SO4+2CH3COOH
���������
�����Ѷȣ�����