时间:2019-05-30 04:53:10
1、选择题 配制100mL?1.0mol?L-1的Na2CO3溶液,下列情况会导致溶液浓度偏高的是( )
A.容量瓶使用前用1.0?mol?L-1的Na2CO3溶液润洗
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.仰视确定凹液面与刻度线相切
D.用敞口容器称量Na2CO3且时间过长
2、选择题 配制一定物质的量浓度的KOH溶液时,造成最终浓度偏低的原因可能是( )
A.容量瓶事先没有烘干
B.定容时观察液面俯视
C.定容时观察液面仰视
D.定容后,摇匀时有少量液体流出
3、简答题 实验室制配0.5mol/L的NaOH溶液500mL,有以下仪器:①烧杯?②100mL量筒③1000mL容量瓶?④500mL容量瓶?⑤玻璃棒?⑥试管?⑦药匙
(1)配制时,必须使用的仪器有______(填代号)还缺少的仪器是______.
(2)实验两次用到玻璃棒,其作用分别是:______、______.
(3)配制时,一般可分为以下几个步骤:①称量?②计算?③溶解?④摇匀⑤转移⑥洗涤?⑦定容?⑧冷却.其正确的操作顺序为______.
(4)试分析下列操作对所配溶液的浓度有何影响.(填“偏高”、“偏低”或“无影响”)
①定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,对所配溶液浓度的影响______.
②某同学观察液面的情况如图所示,则所配置的溶液的浓度______.
(5)取出其中50ml溶液加水稀释到100ml,稀释后溶液中NaOH的物质的量浓度为______.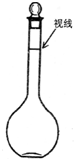
4、填空题 现需配制0.2mol/LNaHCO3?溶液450mL,某同学如图转移溶液.
①图中的错误是______
②实验中应选择容量瓶的规格是______(选填100mL或500mL);实验时需称取NaHCO3的质量为______g
③配制时,其正确的操作顺序是______(字母表示,每个字母用且只能用一次).
A、每次用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B、准确称取计算量的固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C将溶解后的溶液沿玻璃棒注入容量瓶中
D、将容量瓶盖紧,振荡,摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F、继续往容易瓶内小心加水,直接液面接近刻度2~3cm处.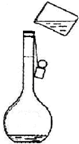
5、填空题 实验室用固体烧碱配制500 mL 0.1 mol·L-1的NaOH溶液。
(1)需称量________g烧碱固体,它应该放在________中进行称量。
(2)配制过程中,不需要使用的仪器是(填写代号)________。
A.烧杯 B.量筒 C.1000 mL容量瓶 D.托盘天平
E.药匙 F.500 mL容量瓶 G.胶头滴管 H.漏斗
(3)除上述可使用的仪器,还缺少的仪器是_________,它在实验中的作用为_______。
(4)要配制浓度约为2mol·L-1NaOH溶液100mL,下列操作正确的是________。
①称取8g NaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解。
②称取8g NaOH固体,放入100mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完 全溶解后用蒸馏水稀释至100 mL。
③称取8g NaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加水至刻度线,塞好瓶塞,反复摇匀。
④用100mL量筒量取40mL 5 mol·L-1 NaOH,倒入250mL烧杯中,再用同一量筒量取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中。