时间:2019-05-30 04:16:15
1、简答题 已知下列热化学方程式:
(1)C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
(2)2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-1
(3)2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2599kJ?mol-1
请写出C(s,石墨)和H2(g)生成1mol C2H2(g)的热化学方程式______.
参考答案:(1)C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
(2)2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ?mol-1
(3)2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2599kJ?mol-1
利用盖斯定律将(1)-(2)2-(3)2可得:
2C(s,石墨)+H2(g)=C2H2(g)△H=(-393.5kJ/mol)-2×(-571.6kJ/mol)-(-2599 kJ/mol)=+226.7kJ?mol-1,
所以热化学反应方程式为:2C(s,石墨)+H2(g)=C2H2(g);△H=+226.7kJ?mol-1
故答案为:2C(s,石墨)+H2(g)=C2H2(g);△H=+226.7kJ?mol-1.
本题解析:
本题难度:一般
2、选择题 已知101KPa时辛烷的标准燃烧热为—5518kJ·mol-1,含20gNaOH的稀溶液与稀盐酸充分反应放出热量28.7kJ,则下列热化学方程式书写正确的是
①C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(g); △H = +5518 kJ·mol-1
②C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(l); △H = -5518 kJ·mol-1
③H+(aq)+ OH-(aq)= H2O(l); △H = -57.4 kJ·mol-1
④HCl (aq) + NaOH(aq) =NaCl(aq) + H2O(l); △H = —28.7 kJ·mol-1
A.①③
B.②③
C.②④
D.②
参考答案:B
本题解析:燃烧热是1mol可燃物完全燃烧生成稳定的氧化物所放出的热量,焓变小于零,②正确;中和热是强酸与强碱中和生成1mol水时放出的热量,20g氢氧化钠是0.5mol,放热28.7kJ,③正确;答案选B。
考点:燃烧热、中和热
本题难度:一般
3、填空题 (15分)甲醇可作为燃料电池的原料。工业上利用CO2和H2在一定条件下反应合成甲醇。
(1)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(2)甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题: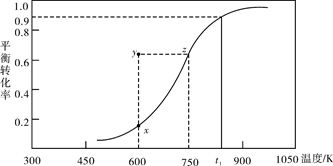
①600K时,Y点甲醇的υ(逆) (正)(填“>”或“<”)
②从Y点到X点可采取的措施是______________________________________。
③有同学计算得到在t1K时,该反应的平衡常数为8.1mol·L-1。你认为正确吗?请说明理由 。
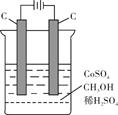
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(Ⅰ)和(Ⅱ)分别进行催化CH3OH的脱氢实验:CH3OH(g) HCHO(g)+H2(g)
HCHO(g)+H2(g)
CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
参考答案:(15分)
(1)CH3OH(l)+ O2(g) = CO(g) + 2H2O(l) ΔH=
本题解析:
本题难度:困难
4、选择题 用CH4催化还原NOx可以消除氮氧化物的污染。已知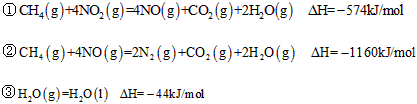
下列说法不正确的是
[? ]
A.等物质的量的CH4参加反应,反应①②转移的电子数相同
B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l);⊿H=-618KJ/mol
C.0.2 mol CH4还原NO2至N2,且生成H2O(g)放出的热量为173.4kJ
D.若用4.48 L(标准状况)CH4还原NO2至N2,整个过程中转移电子1.60mol
参考答案:B
本题解析:
本题难度:一般
5、填空题 (6分)红磷(P)和白磷(P4)均为磷的同素异形体。已知:
P4 ( 白s )+ 5O2 ( g )= P4O10( s ) △H =" -2983.2" kJ/mol
P(红 s )+ 5/4O2 ( g )= 1/4P4O10( s ) △H =" -738.5" kJ/mol
写出白磷转化为红磷的热化学方程式 ,由此可知,红磷比白磷 。(填“稳定”或“不稳定”)
参考答案:(6分)P4(s)=4P(s) △H=-29.2 kJ/mol,稳定;
本题解析:由盖斯定律,第一个热化学方程式减去4倍第二个热化学方程式得,P4 ( 白s )=P(红 s ) △H=" -2983.2" kJ/mol-(-738.5 kJ/mol)×4=-29.2 kJ/mol,由此可知,白磷具有的能量高,红磷比白磷稳定。
考点:热化学方程式的书写
本题难度:一般