时间:2019-05-30 04:10:09
1、选择题 下列现象与氢键有关的是
①NH3的熔、沸点比VA族其他元素氢化物的高
②小分子的醇、羧酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
A.①②③④⑤
B.①②③⑤
C.①②③④
D.①②③
参考答案:B
本题解析:
答案:B
④水分子高温下也很稳定,是由水分子中H―O键键能大决定的,与氢键无关。
①氨气分子之间形成氢键,使分子间作用力增大,NH3的熔、沸点比VA族其他元素氢化物的高
②小分子的醇、羧酸分子之间以及与水分子之间形成氢键,可以和水以任意比互溶
③水分子结成冰,冰的水分子之间以氢键相互作用,形成有规律的排列,分子间空隙增大,冰的密度比液态水的密度小
⑤邻羟基苯甲酸分子内形成氢键,使分子间作用力减弱,邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
本题难度:一般
2、选择题 下列说法正确的是(?)
A.有些物质是由原子直接构成,如水晶、金刚砂等;有些物质是由分子直接构成,如干冰、明矾等;有些物质是由离子直接构成的,如皓矾、芒硝等
B.BF3、H2O、SiCl4、PCl5四种分子中所有原子都满足最外层8电子结构
C.非金属氧化物不都是酸性氧化物;金属氧化物不都是碱性氧化物
D.尿素的熔点比醋酸的熔点高,这是由于前者比后者有更大的范德华力所致
参考答案:C
本题解析:明矾为离子化合物,是由离子构成的物质,A项正确;BF3中B的最外层为6电子结构、PCl5中P的最外层为10电子结构,B项错误;不成盐的非金属氧化物(NO、CO)都不是酸性氧化物、两性氧化物(Al2O3)不是碱性氧化物,C项正确;尿素和醋酸的相对分子质量相等,范德华力相等,故熔点差异不源于此,D项错误。
本题难度:一般
3、选择题 下列说法正确的是
[? ]
A.凡金属跟非金属元素化合时都形成离子键
B.离子化合物中,一个阴离子可同时与多个阳离子有静电作用
C.离子化合物中的阳离子只能是金属离子
D.溶于水可以导电的化合物一定是离子化合物
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列有关叙述中正确的是
[? ]
A.由碳、氮原子形成的化合物比金刚石坚硬,其主要原因是碳氮键比碳碳键短
B.液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
C.S8和NO2都是共价化合物,NH4Cl和CaC2都是离子化合物
D.若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数有可能为m+10
参考答案:A
本题解析:
本题难度:简单
5、填空题 过氧化氢(H2O2)的水溶液俗称双氧水,其水溶液可用于制备工业上的漂白剂、特殊环境里燃料燃烧的助燃剂、医疗上的消毒剂、实验室里的制氧剂;过氧化钠(Na2O2)可用于制备工业上的漂白剂、特殊环境里的供氧剂、实验室里的制氧剂。过氧原子团“O2”由2个氧原子共用1对电子组成。 ?
(1)分别写出H2O、Na2O2的电子式:_______、________。 ?
(2)①H2O、H2O2中化学键的不同点是_________________;
②Na2O、Na2O2中化学键的不同点是_________________; ?
③H2O2、Na2O2的化合物类型是(共价化合物、离子化合物)__________________。 ?
(3)分别写出H2O2、Na2O2作供氧剂的化学反应方程式
H2O2:___________________;Na2O2:_______________________。 ?
(4)H2O2与Na2O2相比,化学键更稳定的是(写物质的名称)_______,主要根据是___________________________。?
参考答案:(1)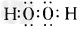 ;
;
(2)①H2O中没有非极性键,H2O2中有非极性键;?②Na2O中没有共价键,Na2O2中有共价键(或非极性键)?;③H2O2是共价化合物,Na2O2是离子化合物?
(3)2H2O2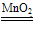 2H2O+O2↑;2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2= 2Na2CO3+O2?
2H2O+O2↑;2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2= 2Na2CO3+O2?
(4)过氧化氢;Na2O2在常温下跟水快速反应生成O2,H2O2的水溶液在催化剂作用下才能较快地反应生成O2
本题解析:
本题难度:一般