时间:2019-05-30 04:07:21
1、选择题 有A、B、C、D四种金属。将A与B用导线连结起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度的盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们活动性由强到弱的顺序是
[? ]
A.D>C>A>B
B.D>A>B>C
C.D>B>A>C
D.B>A>D>C
参考答案:B
本题解析:
本题难度:一般
2、实验题 如下两个反应: A、NaOH+HCl=NaCl+H2O? B、2FeCl3+Fe=3FeCl2
(1)根据两反应本质,分别判断能否用于设计原电池____________________________。其理由_________________________________________________________。
(2)如果可以,请画出实验装置图,注明电解质溶液名称和正负极材料,标出电子的流动方向,写出电极反应式。

________是正极,正极反应式:___________________;
________是负极,负极反应式:__________________。
参考答案:(1)(A)不行(B)可以,(A)不是氧化还原反应,没有发生电子的转移
(2)实验装置图如右图所示:
Cu(或C)是正极,正极反应式:2Fe3++2e-=2Fe2+
Fe是负极,负极反应式:Fe-2e-=Fe2+
本题解析:判断能否设计原电池的原理是该反应能否发生氧化还原反应,有无电子转移,依题意可知A不行,B有电子转移,故可以。

依据不活泼物质如Cu或C做正极Cu(或C)是正极,正极反应式:2Fe3++2e-=2Fe2+
活泼的金属如Fe容易失去电子做负极,负极反应式:Fe-2e-=Fe2+
点评:原电池是高中化学的重点也是难点,考生要着重掌握原电池设计原理,从本质上去理解从而真正地掌握,培养发散思维能力。
本题难度:一般
3、简答题 分废旧铅蓄电池的回收利用是发展循环经济的必经之路。其阴、阳极填充物(铅膏,主要含PbO、PbO2、PbSO4)是废旧铅蓄电池的主要部分,回收时所得黄丹(PbO)、碳酸铅可用于合成三盐基硫酸铅(组成可表示为3PbO・PbSO4・H2O),其工艺流程如下:
(1)用碳酸盐作转化剂,将铅膏中的硫酸铅转化为碳酸铅,转化反应式如下:
PbSO4(s)+CO ?(aq)
?(aq) PbCO3(s)+SO42-(aq)
PbCO3(s)+SO42-(aq)
①下列说法错误的是:___________________。
A.PbSO4的Ksp比PbCO3的Ksp大
B.该反应平衡时,c(CO )=c(SO42-)
)=c(SO42-)
C.该反应的平衡常数K= ?
?
②室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化,在_________溶液中PbSO4转化率较大,理由是_________。
(2)滤液A能用来回收Na2SO4・10H2O,提取该晶体的主要步骤有____________、___________、过滤、洗涤、干燥;检验该晶体中阴离子的实验方法是______________。
(3)物质X是一种可循环使用的物质,其溶质主要是______________(填化学式),若X中残留的SO过,循环利用时可能出现的问题是__________________。
(4)生成三盐基硫酸铅的离子方程式为____________________。
(5)向铅膏浆液中加入Na2SO3溶液的目的是将其中的PbO2还原为PbO。若实验中所取铅膏的质量为47.8g,其中PbO2的质量分数为15%,则要将PbO2全部还原,至少需要加入__________mL的0.5 mol・L-1 Na2SO3溶液。
参考答案:(1) ①B(2分)?②Na2CO3(1分);相同浓度的Na2CO3和NaHCO3溶液中,前者c(CO32-)较大?(1分)
(2)蒸发浓缩(1分)、冷却结晶(1分) ?取少量晶体溶于蒸馏水,然后用盐酸酸化,再滴BaCl2溶液,若出现白色沉淀,即证明该晶体中含有SO42- (2分)
(3)HNO3(1分)浸出时部分铅离子生成PbSO4随浸出渣排出,降低PbSO4的产率(2分)
(4)4 PbSO4 + 6OH- ="3" PbO・PbSO4・H2O + 3 SO42- + 2 H2O? (2分)?
(5) 60(2分)
本题解析:(1) ①对于PbSO4(s)+CO (aq)
(aq) PbCO3(s)+SO42-(aq)可知:
PbCO3(s)+SO42-(aq)可知:
反应的平衡常数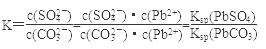
根据转化关系可知PbSO4的Ksp比PbCO3的Ksp大,A正确;当K=1,平衡时才有c(CO )=c(SO42-),B不正确;C正确。
)=c(SO42-),B不正确;C正确。
②室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化,前者c(CO32-)较大, PbSO4转化率较大。
(2)滤液A能用来回收Na2SO4・10H2O,提取该晶体的主要步骤有干燥蒸发浓缩、冷却结晶、过滤、洗涤;检验该晶体中SO42-的实验方法是取少量晶体溶于蒸馏水,然后用盐酸酸化,再滴BaCl2溶液,若出现白色沉淀,即证明该晶体中含有SO42-。
(3)可循环使用的物质HNO3;若HNO3中残留的SO42-过多,循环利用时可能出现的问题是浸出时部分铅离子生成PbSO4随浸出渣排出,降低PbSO4的产率;
(5)由于:Na2SO3+PbO2===PbO+ Na2SO4可知:n(Na2SO3)=n(PbO2)=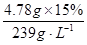 ?=0.03mol,故需要加入60mL的0.5 mol・L-1 Na2SO3溶液。
?=0.03mol,故需要加入60mL的0.5 mol・L-1 Na2SO3溶液。
本题难度:一般
4、填空题 理论上任何自发的氧化还原反应都可以设计成原电池。现使用锌电极、铜电极、橙子(酸性介质)设计如下水果电池。? 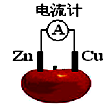
(1)该电池的负极材料是__________,负极反应式:____________;
(2)现有如下材料设计类似的水果电池,并使电流计发生明显偏转。
酸性水果:柠檬、柑橘、橙子等
碱性水果:柿子、葡萄等
电极:A.镁条、B.铝片、C.铜片、D.碳棒。
①若选择酸性水果组装水果电池,负极材料可以是:___________(填所有可能的电极选项)正极反应式为:____________
②若选择碱性水果组装水果电池,正极材料可以是:____________(填所有可能的电极选项)假设水果的碱性较强,电池的负极反应式为:_____________?
(3)原电池的电解质溶液也可以呈中性,例如为海洋中的航行灯提供电能的就是由铝、空气、海水构成的原电池,该电池总反应为4Al+3O2+6H2O=?4Al(OH)3,写出该电池的正极反应式___________。
参考答案:(1)?锌或Zn ;Zn-2e-=Zn2+?
(2)?①:AB;2H++2e-=H2↑; ②:ABD;Al-3e-+4OH-=?AlO2-+2H2O
(3)?O2+4e-+2H2O=?4OH-
本题解析:
本题难度:一般
5、选择题 某原电池工作时总的反应为Zn+Cu2+===Zn2++Cu,该原电池的组成可能是?
A.Zn为正极,Cu为负极,CuCl2溶液作电解质溶液
B.Cu为正极,Zn为负极,稀H2SO4作电解质溶液
C.Cu为正极,Zn为负极,CuSO4溶液作电解质溶液
D.Fe为正极,Zn为负极,CuCl2溶液作电解质溶液
参考答案:CD
本题解析:把电池反应方程式拆成两个半电池,发生氧化反应的电极为负极,所以锌作负极;发生还原反应的电极为正极,所以用不如锌活泼的金属或非金属导体作正极;含有发生还原反应的离子溶液为电解质溶液,所以是含有铜离子的溶液.
故选CD.
本题难度:一般