时间:2019-05-30 03:54:30
1、填空题 (5分)有铜片、锌片、若干小烧杯、导线、、盐桥(含琼胶的KCl饱和溶液)、电流计、ZnSO4溶液、CuSO4溶液,试画出原电池的装置图,并说明其工作原理。
⑴原电池装置图;?⑵工作原理;
参考答案:⑴原电池的装置图(3分)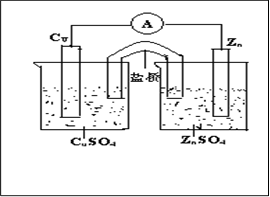
⑵工作原理(2分):
负极锌失电子,发生了氧化反应,使负极区域多出了Zn2+,盐桥向该池中传递带等量负电荷的Clˉ,电子沿导线传递到正极,正极带负电,吸引阳离子CU2+,CU2+在该电极得电子发生还原反应,使正极区域多出了负离子SO42ˉ,盐桥向该池中传递带等量正电荷的K+。
本题解析:略
本题难度:一般
2、选择题 X、Y、Z、M四种金属,已知X可以从Y的盐溶液中置换出Y;X和Z作原电池电极时,Z为正极;Y和Z的离子共存于电解液中,Y离子先放电;M的离子的氧化性强于Y的离子。则这四种金属的活动性由强到弱的顺序为下列的
[? ]
A.X>Y>Z> M
B.X>Z>M>Y
C.M>Z>X>Y
D.X>Z>Y>M
参考答案:D
本题解析:
本题难度:一般
3、选择题 一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列说法中正确的是
A.正极上发生的反应为:O2+ 2H2O + 4e-= 4OH-
B.电池反应的化学方程式为:CH3CH2OH+ O2=CH3COOH+H2O
C.检测时,溶液中的H+向负极移动
D.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
参考答案:B
本题解析:酸性燃料电池,正极上的反应不可能生成OH-,正极反应为:O2 + 4e- = 4H++ 2H2O,A错误;溶液中正离子H+向正极移动,C错误;若有0.4mol电子转移,则消耗0.1mol O2,标况下为2.24L,D错误。
考点:原电池
点评:该题是高考中的常见题型,试题基础性强,注重考查学生分析问题、解决问题的能力。该题的关键是理解原电池和电解池的工作原理,会熟练书写电极反应式,然后结合题干灵活分析即可。
本题难度:一般
4、简答题 根据以下实验装置和现象填写实验报告(A、B、C、D为四种金属)
| 装置 |  |  |  现象 B棒有气泡 C棒有Cu析出 A棒附近PH升高 ① ② ③ |
| 四种金属活动性由强到弱的顺序:______ 参考答案:①B棒上有气泡发生,说明B棒上发生还原反应生成氢气,则B棒为原电池的正极,A为负极,活泼性A>B, 本题解析: 本题难度:一般 5、填空题 氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电 参考答案:(1)由化学能转化为电能 (2)由a到b 本题解析:(1)根据原电池的工作原理可知,氢氧燃料电池的能量转化形式主要是由化学能转化为电能。 本题难度:简单 | |||