时间:2019-05-30 03:54:30
1、填空题 (3分)请根据反应Fe+CuSO4==Cu+FeSO4设计一个原电池,画出装置图
参考答案:略
本题解析:略
本题难度:简单
2、选择题 如图所示是一个燃料电池的示意图,当此燃料电池工作时,下列分析中正确的是
A.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上发生的反应为:H2-2e-=2H+
B.如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通O2的电极上发生的反应为:O2+4e-+2H2O=4OH-
C.如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则通CH4的电极上发生的反应为:CH4-8e-+10 OH-=CO +7H2O
+7H2O
D.如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则溶液中的OH-离子向b极附近移动
参考答案:C
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。A不正确,电解质是氢氧化钠,负极反应式为H2-2e-+2OH-=2H2O。B不正确,因为电解质是硫酸,所以正极反应式为O2+4e-+4H+=2H2O。C正确,D中b极是正极,阴离子阴离子向负极移动,D不正确,答案选C。
本题难度:一般
3、选择题 下列关于充电电池的叙述,不正确的是( )
A.充电电池的化学反应原理是氧化还原反应
B.充电电池可以无限制的反复使用
C.充电是使放电的氧化还原反应逆向进行
D.较长时间不使用电器时,最好从电器中取出电池,并妥善存放
参考答案:A、充电电池的化学反应有化合价的变化,所以是氧化还原反应,故A正确.
B、充电电池属于二次电池,但并不是可以无限制地反复充电、放电,故B错误.
C、充电过程的反应物是放电过程的生成物,所以充电是使放电的氧化还原反应逆向进行,故C正确.
D、果用电器较长时期内不再使用,最好将电池取出并放于低温,干燥的地方,如果不这样,即使用电器被关掉,系统仍会使电池有一个低电流输出,这会缩短电池的使用寿命,故D正确.
故选B.
本题解析:
本题难度:一般
4、选择题 用石墨做电极,电解氯化铜和氯化钠的混合溶液,在任何情况下,阴、阳两极下不可能同时发生的反应是( )
A.阴极:2H++2e-=H2↑?阳极:4OH--4e-=2H2O+O2↑
B.阴极:2H++2e-=H2↑?阳极:2Cl--2e-=Cl2↑
C.阴极:Cu2++2e-=Cu?阳极:4OH--4e-=2H2O+O2↑
D.阴极:Cu2++2e-=Cu?阳极:2Cl--2e-=Cl2↑
参考答案:C
本题解析:
本题难度:简单
5、填空题 Ⅰ.在下图的装置中,属于原电池的是??。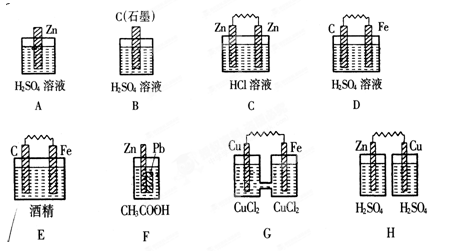
Ⅱ.(1)如图所示,烧杯中为CuCl2溶液,在图中画出必要的连线或装置,使连接后的装置为原电池。电极反应方程式: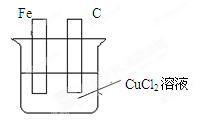
铁板:?;碳棒:?。
(2)铜片、锌片连接后浸入稀硫酸中构成原电池,当导线上通过3.01×1022个电子时,锌片质量减少________g。铜片表面析出氢气_________L(标准状况)。
参考答案:Ⅰ.D、F、G?Ⅱ.(1)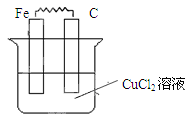 Fe-2e-=Fe2+? Cu2++2e-=Cu
Fe-2e-=Fe2+? Cu2++2e-=Cu
(2)1.625g? 0.56L
本题解析:Ⅰ.原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,据此可知:
A、该装置只有一个电极材料,所以不能形成原电池;
B、该装置只有一个电极材料,且石墨和电解质溶液不能自发的进行氧化还原反应,所以不能形成原电池;
C、两电极材料相同,所以不能形成原电池,故错误;
D、该装置符合原电池的构成条件,所以能形成原电池,故正确;
E、酒精不是电解质,铁和酒精不能自发的进行氧化还原反应,所以不能形成原电池;
F、该装置符合原电池的构成条件,所以能形成原电池,故正确;
G、该装置符合原电池的构成条件,所以能形成原电池,故正确;
H、该装置两电极间不能构成闭合回路,所以不能形成原电池,所以答案选D、F、G
Ⅱ.(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。铁是活泼的金属,所以铁是负极,碳棒是正极,溶液中的铜离子再正极得到电子,发生还原反应,电极反应式分别是Fe-2e-=Fe2+、Cu2++2e-=Cu。
(2)铜片、锌片连接后浸入稀硫酸中构成原电池,其中锌是负极,铜是正极,电极反应式分别是Zn-2e-=Zn2+、2H++2e-=H2↑。3.01×1022个电子的物质的量是3.01×1022÷6.02×1023/mol=0.05mol,所以锌片质量减少0.025mol×65g/mol=1.625g,铜片表面析出氢气的体积(标准状况下)是0.025mol×22.4L/mol=0.56L。
点评:该题是高考中的常见考点,侧重对学生基础知识的巩固和训练。有利于培养学生的逻辑推理能力和规范答题能力。明确原电池的工作原理、构成条件是答题的关键,注意相关知识的积累和总结。
本题难度:一般