时间:2019-05-30 03:29:47
1、填空题 (12分)
A.原子数相同、电子总数相同的分子,互称为等电子体。
Ⅰ.已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、6和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1 :2。
请回答:
(1)组成A分子的原子的元素符号是?;已知E是有毒的有机物,E的熔、沸点比CH4的熔、沸点高,其主要原因是____________________________________。
(2)C的立体结构呈?____ 形,该分子属于?分子(填“极性”或“非极性”);
(3)火箭中可充入四氧化二氮和D作为燃料反应生成氮气和水,该反应的化学方程式为_______?__________________。(不需要写反应条件)
Ⅱ.CO与N2互为等电子体。
(4)CO的总键能大于N2的总键能,但CO比N2容易参加化学反应。
根据下表数据,说明CO比N2活泼的原因是____________________________________。
| ? | ? | A-B | A=B | A≡B |
| CO | 键能(kJ/mol) | 357.7 | 798.9 | 1071.9 |
| 键能差值kJ/mol) | ? 441.2? 273 | |||
| N2 | 键能(kJ/mol) | 154.8 | 418.4 | 941.7 |
| 键能差值kJ/mol) | ? 263.6? 523.3 | |||
2、选择题 下列说法正确的是
A.苯分子中含有三个碳碳双键
B.将乙酸和乙醇混合加热即可制取乙酸乙酯
C.葡萄糖能够发生银镜反应
D.糖类、油脂、蛋白质均能发生水解
3、填空题 (12分)已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2―离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2。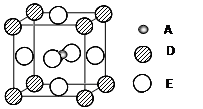
 请回答下列问题:
请回答下列问题:
⑴A、B、C、D四种元素中,电负性最大的是?▲?(填元素符号)。
⑵B的氢化物的沸点远高于A的氢化物的主要原因是?▲?。
⑶由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为?▲?。
⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有?▲?。
⑸最近发现,只含A、D、E三种元素的一种晶体(晶胞如右图所示)具有超导性。A原子的配位数为?▲?;该晶体的化学式为?▲?。
4、选择题 S2Cl2是橙黄色液体,少量泄漏会产生室息性气味的气体,喷水雾可减慢挥发,并产生酸性悬浊液。其分子结构如图所示。下列关于S2Cl2的说法错误的是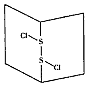
[? ]
A.为非极性分子
B.分子中既含有极性键又含有非极性键
C.与S2Br2结构相似,熔沸点S2Br2>S2Cl2
D.与水反应的化学方程式可能为2S2Cl2+2H2O=SO2↑+3S↓+4HCl
5、简答题 现有10种元素的性质、数据如下表所列,它们均为短周期元素.
| A | B | C | D | E | F | G | H | I | J 原子半径(10-10m) 0.74 1.60 1.52 1.10 0.99 1.86 0.75 0.82 0.102 0.037 | |
| 最高或最低 化合价 +2 +1 +5 +7 +1 +5 +3 +6 +1 -2 -3 -1 -3 -2 |