时间:2019-05-30 03:26:02
1、选择题 为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是
(1)过滤?(2)加过量的NaOH溶液 (3)加适量HCl (4)加过量的Na2CO3溶液
(5)加过量的BaCl2溶液
A.(2)(3)(4)(5)(1)
B.(4)(1)(2)(5)(3)
C.(2)(5)(4)(1)(3)
D.(5)(2)(4)(3)(1)
参考答案:C
本题解析:Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,最后加入盐酸酸化。但用于过量的氯化钡要用碳酸钠来除,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠可以随意调整,因此正确的顺序可以是②⑤④①③,答案选C。
本题难度:一般
2、填空题 为了达到下表所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入答题卡中。
供选择的化学试剂:
A.酸性高锰酸钾
B.硝酸银溶液和硝酸
C.氢氧化钠溶液
D.无水硫酸铜粉末
| 实验要求 | 化学试剂 |
| 检验酒精中是否有水 | ? |
| 区别CH4和C2H4两种无色气体 | ? |
| 验证味精是否有食盐 | ? |
| 除去Fe2O3中的Al2O3 | ? |
参考答案:(4分)D ?A ?B ?C
本题解析:略
本题难度:一般
3、选择题 用括号内试剂和方法除去下列各物质中的少量杂质,正确的是(?)
A.乙烷中的乙烯(酸性高锰酸钾溶液,洗气)
B.苯中的苯酚(浓Br2水,过滤)
C.乙醇中的水(新制的CaO,过滤)
D.乙酸乙酯中的乙酸(饱和Na2CO3溶液,分液)
参考答案:D
本题解析:酸性高锰酸钾溶液氧化乙烯得到CO2杂质,苯酚与浓Br2水反应生成的沉淀不溶于水但是可溶于苯,AB错误。乙醇中的水用新制的CaO吸水,然后蒸馏得到乙醇。
本题难度:一般
4、实验题 环己酮是一种重要的有机化工原料。实验室合成环己酮的反应如下: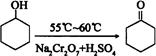
环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g・cm―3、20 ℃) | 溶解性 | ? |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 | |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 | ? |

参考答案:(1)D B E C A
(2)使水层中少量的有机物进一步被提取,提高产品的产量
(3)A B C
(4)降低环己酮的溶解度;增加水层的密度,有利于分层?水浴加热
(5)停止加热,冷却后通自来水
(6)60%(60.3%)
本题解析:(1)在上述方法中制取的物质环己酮中含有未反应的环己醇。由于环己醇能溶于水和醚,而环己酮微溶于水,能溶于醚,所以提纯步骤的正确步骤首先是往液体中加入NaCl固体至饱和,静置,分液。然后水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层;再加入无水MgSO4固体,除去有机物中少量水。接着进行过滤,除去MgSO4晶体。最后蒸馏、除去乙醚后,收集151℃~156℃馏分即得到纯净的环己酮。(2)在B中水层用乙醚萃取的目的是使水层中少量的有机物进一步被提取,提高产品的产量。(3)混合振荡:用左手握住分液漏斗活塞,右手压住分液漏斗口部,把分液漏斗倒转过来振荡,使两种液体充分接触,振荡后打开活塞,将漏斗内气体放出. 分液时,为了使液体能够顺利流出,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,下层液体从下口流出,上层的液体从上口倒出。因此,错误的操作为A B C 。(4)在上述操作D中,加入NaCl固体的作用是降低环己酮的溶解度;增加水层的密度,有利于分层。在蒸馏除乙醚的操作中为了减少环己酮的挥发造成的消耗。通常采用的加热方式为水浴加热。(5)蒸馏操作时,一段时间后若发现未通冷凝水,应采取的正确方法是停止加热,冷却后通自来水,否则会导致冷凝管炸裂。(6)实际产量:m(环己酮)=" 0.9478g/ml×12mL=" 11.3736g.n(环己酮)=m÷M=11.3736g÷98g/mol="0.116mol." m(环己醇)= 0.9624g/ml×20ml=19.248g.n(环己醇)=19.248g ÷100g/mol="0.19248mol" .所以环己酮的产率为:(0.116mol÷0.19248mol)×100% ="60%" 。
本题难度:一般
5、填空题 现有一包氯化钠固体,其中混有少量的硫酸钠和氯化镁,可通过以下实验除去杂质得到纯净的氯化钠。
(1)请将正确合理的操作顺序填入括号中
( )在溶液中加入稍过量的碳酸钠溶液,然后过滤。
( )加入稍过量的氯化钡溶液,然后过滤。
( )在滤液中加入稀盐酸至溶液呈中性。
( )将混有杂质的氯化钠完全溶解于水。
( )蒸发结晶。
( )在滤液中加入稍过量的氢氧化钠溶液,然后过滤。
(2)为什么要加入稍过量的碳酸钠溶液?____
(3)为什么要加入稀盐酸至溶液呈中性?____
(4)写出上述两步骤中的有关化学方程式____。
参考答案:(1)③②⑤①⑥④
(2)为了除去溶液中多余的钡离子
(3)为了除去过量的碳酸根和氢氧根
(4)Na2CO3+BaCl2=BaCO3↓+2NaCl, Na2CO3+2HCl=2NaCl+CO2↑+H2O, NaOH+HCl=NaCl+H2O
本题解析:
本题难度:一般