ʱ��:2019-05-30 03:03:59
1������� ���ݣ�NH4��2CO3��aq���д��ڵ����������ӣ�������������⣺
��1�����ݵ���غ㣬д��һ��������Ũ�ȱ�ʾ�ĵ�ʽ��______��
��2������ˮ�ĵ��룬д��һ������[H+]��[OH-]�ĵ�ʽ��______��
��3�����ݣ�NH4��2CO3�У�C��Nԭ�Ӹ�����ϵ��д��һ������[NH4+]��[CO32-]�ĵ�ʽ��______��
�ο��𰸣���1���κ���Һ�ж����ڵ���غ㣬����Һ�д���CO32-��HCO3-��OH-��NH4+��H+�����ݵ���غ�c�� NH4+��+c��H+��=c��OH-��+c��HCO3-��+2c��CO32-����
�ʴ�Ϊ��c�� NH4+��+c��H+��=c��OH-��+c��HCO3-��+2c��CO32-����
��2��ˮ�������H+��OH-����ȵģ���ˮ�������H+��ȫ�������Ĵ�������Һ�У��еĴ����� HCO3-�У��еĴ�����H2CO3������ˮ�������H+��������Ũ����ʽ��ʾΪ��c��H+��+c�� HCO3-��+2c��H2CO3����ͬ����ˮ�������OH-Ҳ��ȫ��������������Һ�У��еĺ�NH4+��ϴ�����NH3?H2O�У���NH+4��ϵ�OH-�������ǽ�����ɵ�NH3?H2O������ȵģ�����ˮ�������OH-����������Ũ����ʽ��ʾΪ��c��OH-��+c��NH3?H2O��������������غ��c��H+��+c�� HCO3-��+2c��H2CO3��=c��OH-��+c��NH3?H2O����
�ʴ�Ϊ��c��H+��+c�� HCO3-��+2c��H2CO3��=c��OH-��+c��NH3?H2O����
��3����NH4��2CO3�У�N��N����N��C��=2��1����NH4��2CO3�е�Nԭ�ӣ��еĴ�����NH4+�У��еĴ�����NH3?H2O�У���������Ũ����ʽ�ɱ�ʾΪ��cc����NH4+��+c��NH3?H2O������NH4��2CO3�е�Cԭ�ӣ��еĴ�����CO32-���еĴ����� HCO3-�У����еĴ�����H2CO3�У���������Ũ����ʽ�ɱ�ʾΪ��c��CO32-��+c�� HCO3-��+c��H2CO3����
���������غ��c�� NH4+��+c��NH3?H2O��=2c��CO32-��+2c�� HCO3-��+2c��H2CO3����
�ʴ�Ϊ��c�� NH4+��+c��NH3?H2O��=2c��CO32-��+2c�� HCO3-��+2c��H2CO3����
���������
�����Ѷȣ���
2��ѡ���� ����˵��������ǣ�������
A����Һ����������ֱ��С��10-9m
B��ʯ�ࡢâ�����̷����dz�����������
C���������������Һ��Ϻ��䵼������һ������
D������ʹ�������ж����������������ˮ��ʱ������Կ���
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� ���е��뷽��ʽ�У�������ǣ�?
A��H2CO3 H++HCO3�� HCO3��
H++HCO3�� HCO3�� H++CO32��
H++CO32��
B��NaHS = Na++H++S2��
C��H2SO4 = 2H++SO42��
D��CH3COOH  H�� + CH3COO�D
H�� + CH3COO�D
�ο��𰸣�B
������������⻯�����������ʽ�Σ����뷽��ʽΪNaHS�� Na++HS����B����ȷ���������ȷ�ģ���ѡB��
�����Ѷȣ���
4��ѡ���� �����Va��0.1mol?L-1HCl��Һ�м������Vb��0.1mol?L-1��ˮ����ϵ�����ǣ�������
A��Va��Vbʱ��c��NH3?H2O��+c��NH4+����c��Cl-��
B��Va��Vbʱ��c��NH4+����c��Cl-����c��H+����c��OH-��
C��Va=Vbʱ��c��NH3?H2O��+c��OH-��=c��H+��
D��Va��Vb�����ʱ��c��NH4+��+c��H+��=c��OH-��+c��Cl-��
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5�������
��һ�����£�CH3COOH��Һ�д��ڵ���ƽ�⣺CH3COOH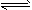 CH3COO-+H+ ��H>0
CH3COO-+H+ ��H>0
��1�����з����У�����ʹ0.10mol��L-1 CH3COOH��Һ��CH3COOH����̶��������____________��
a.��������0.10mol��L-1��ϡ���� b.����CH3COOHc.����ϡ����0.010mol��L-1 d.��������������
e.���������Ȼ��ƹ��� f.��������0.10mol��L-1��NaOH��Һ
��2��25��ʱ���õ���ƽ���ƽ��Ϊ1.75��10-5�����У�
��0.100.010mol��L-1 CH3COOH��Һ ��0.00100.010mol��L-1 CH3COOH��Һ ��c(H+)֮��Ϊ�٣���=______������ʾ�����м��㣬ƽ��ʱ��c(CH3COOH)������ʼŨ�ȴ��棬ˮ�������c(H+)��c(OH-)���Բ��ƣ���ͬ��
��3��25��ʱ����0.10mol��L-1 CH3COOH��Һ�м���һ��������CH3COONa��������Һ������䣩������Һ��c(CH3COO-)Ϊ1.0mol��L-1������Һ��c(H+)=________mol��L-1 ������������С�������λ��Ч���֣�����Һ�и�������Ũ�ȹ�ϵ��_________��
�ο��𰸣���1��bcf
��2��10��1
��3��c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
���������
�����Ѷȣ�һ��